��������1����25��ʱ��0.1mol?L
-1��ij��HA�У����������ǿ�ᣬ��
=10
12��ʵ������
=10
10���Ը��������
�ڼ�ˮϡ�ʹٽ�����룬������Ũ�ȡ���Ũ�ȡ��������Ũ�ȶ����ͣ�������������Ũ������ע��ˮ�����ӻ�����ֻ���¶��йأ�����Һ��������أ�
�ۣ�3��A���������Һ�����ԣ���������Ũ�ȵ�������������Ũ�ȣ�
B��������������ȣ��������ǿ���жϻ����Һ������ԣ�
C�������Һ�����ԣ�����Һ�������������Һ��
D�������Һ�ʼ��ԣ�����Һ�����Ǽ������Һ��Ҳ����ֻ������Һ��
��2���Ȼ���������Һ�д��ڳ����ܽ�ƽ�⣬������Һ�е��ܶȻ��dz�����ֻ���¶ȱ仯�������ܶȻ��ֱ���㣻
��3�����ݷ�Ӧ2SO
2��g��+O
2��g��=2SO
3��g�����1mol SO
2��g������Ϊ1mol SO
3�ġ�H=-99kJ?mol
-1���㷴Ӧ�ȣ�
��4��N
2O
4��g���T2NO
2��g����H��0���÷�ӦΪ���ȷ�Ӧ�������¶ȣ���ѧƽ�������ƶ���NO
2�����������������ѹǿ����ѧƽ�������ƶ���NO
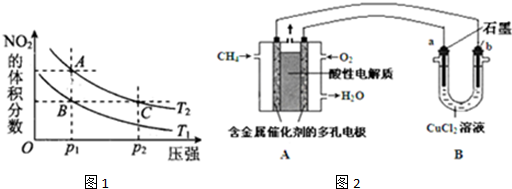
2�����������С�����ͼ�����������
��C���㶼�ڵ������ϣ�ѹǿԽ��Ӧ����Խ�죻
��ѹǿ��ͬ�������¶ȣ���ѧƽ�������ƶ���NO
2�������������A��NO
2�����������
����ͼ���֪��B��C����NO
2�����������ͬ������������ʵ�����ͬ���ݴ��жϣ�
�ܸ����¶Ⱥ�ѹǿ�Է�Ӧ���ʵ�Ӱ�����ش�
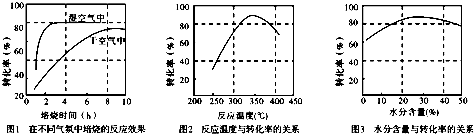
��3����ԭ��ظ�������������Ӧ�������ڸ���ͨ�룬���������£�����������Ӧ����CO
2��H
+��
��BΪ���أ�ͭ���ӷ�����ԭ��Ӧ���������������ü�����ԭ��صĸ���������ת�Ƶ��Ӽ�������Cu�����ʵ������ٸ���m=nM��������Cu��������
���
�⣺��1����25��ʱ��0.1mol?L
-1��ij��HA�У����������ǿ�ᣬ��
=10
12��
=10
10�����Ը��������ᣬ��������ʣ�
�ʴ�Ϊ��������ʣ�
��A����ˮϡ�ʹٽ�����룬������Ũ�ȡ���Ũ�ȡ��������Ũ�ȶ����ͣ���������Ũ�ȼ�С����С������Ӽ�С����������
����A����
B����ˮϡ�ʹٽ�����룬��Ũ�ȡ��������Ũ�ȶ����ͣ����������Ũ�ȼ�С����С������Ӽ�С��������������������Ũ��������
��С����B��ȷ��
C���¶Ȳ��䣬ˮ�����ӻ��������䣬��C����
D����ˮϡ�ʹٽ�����룬������Ũ�Ƚ��ͣ�������������Ũ������D����
�ʴ�Ϊ��B��
�ۣ�3��A���������Һ�����ԣ�����ҺM��c��H
+��=c��OH
-��=1��10
-7 mol?L
-1��������ҺM��c��H
+��+c��OH
-��=2��10
-7 mol?L
-1����A��ȷ��
B����V
1=V
2�������Ũ�ȴ������������ҺM��pHһ��С��7����B����
C�������Һ�����ԣ�����Һ���������Һ���������ᣬ��Ũ�ȴ�����������Ũ�ȣ�����V
1��һ������V
2����C����
D�������Һ�ʼ��ԣ�����Һ�����Ǽ������Һ��Ҳ����ֻ������Һ����V
1һ��С��V
2����D��ȷ��
�ʴ�Ϊ��AD��
��3���Ȼ���������Һ�д��ڳ����ܽ�ƽ�⣬������Ũ��Խ����������Ũ��ԽС��
��100mL����ˮ���Ȼ����γɱ�����Һ��Ag
+Ũ��Ϊ
��10
-5mol/l��
��100mL 0.2mol?L
-1AgNO
3��Һ��Ag
+Ũ��Ϊ0.2mol/l���Ƴ����ܽ�ƽ�⣬
��100mL 0.1mol?L
-1�Ȼ�����Һ��������Ũ��Ϊ0.3mol/L��������Ũ��=6��10
-10mol/L��
��100mL 0.1mol?L
-1������Һ��������Ũ��Ϊ0.1mol/L��������Ϊ1.8��10
-9mol/L��
����������С˳��Ϊ���ڣ��٣��ܣ��ۣ�
�ʴ�Ϊ���ڣ��٣��ܣ��ۣ�
��3����֪��S��s��+O
2��g��=SO
2��g����H
1=-296 KJ?mol
-1����SO
2��g��+
O
2��g��=SO
3��g����H
2=-99 KJ?mol
-1��
�����ø�˹���ɽ��١�3+�ڡ�3�ɵ�3 S��s��+
O
2��g��=3SO
3��g����H
3=3������H
1+��H
2��=-1185 KJ?mol
-1��
�ʴ�Ϊ��-1185 KJ?mol
-1��
��4������ͼ���֪��A��C���㶼�ڵ������ϣ�C��ѹǿ����A��C����ķ�Ӧ���ʣ�A��C���ʢٴ���
��A��C�����¶���ͬ����ѹǿ��ͬ��NO
2Ϊ����ɫ���壬��ͼ���֪��A��NO
2�������������A��C�����������ɫ��A�Cdz���ʢڴ���
����ͼ���֪��B��C����NO
2�����������ͬ������������ʵ�����ͬ������ƽ����Է���������ͬ���ʢ۴���
�������¶ȣ���ѧƽ�������ƶ���NO
2���������������ͼ���֪��A��NO
2�������������T
1��T
2����״̬B��״̬A�������ü��ȵķ������ʢ���ȷ��
�ʴ�Ϊ���ܣ�
��5���١�ԭ��ظ�������������Ӧ�������ڸ���ͨ�룬���������£�����������Ӧ����CO
2��H
+�������缫��ӦʽΪ��CH
4-8e
-+2H
2O=CO
2+8H
+��
�ʴ�Ϊ��CH
4-8e
-+2H
2O=CO
2+8H
+��
�ڡ�BΪ���أ�ͭ���ӷ�����ԭ��Ӧ���������������ü�����ԭ��صĸ���������b�缫����Cu��b�缫���������أ�ת��0.2mol���ӣ�����ͭ�����ʵ���Ϊ
=0.1mol��������ͭ������Ϊ0.1mol��64g/mol=6.4g��
�ʴ�Ϊ��6.4��



 ��ս�п�����ϵ�д�
��ս�п�����ϵ�д�
 ������һ��ǿ������������������������ȣ�
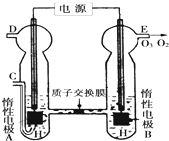
������һ��ǿ������������������������ȣ� TiO2�ڹ����¿�ʹˮ�ֽ⣺2H2O
TiO2�ڹ����¿�ʹˮ�ֽ⣺2H2O