
| A. | 2NO2(g)?N2O4(g),升温时体系颜色加深说明正反应为吸热反应 | |
| B. | N2(g)+3H2(g)?2NH3(g),若升温时NH3的浓度减小,则平衡常数K增大 | |
| C. | CO(g)+H2O(g)?CO2(g)+H2(g),升温时CO的转化率增大,说明正反应为吸热反应 | |
| D. | 反应2HI(g)?H2(g)+I2(g)达到平衡后,增大HI的物质的量,平衡不移动 |
分析 A.升高温度,平衡向吸热方向移动;
B.升高温度,氨气浓度降低,氮气和氢气浓度增大,根据化学平衡常数K=$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2}).{c}^{3}({H}_{2})}$判断;
C.升高温度,平衡向吸热方向移动,据此判断反应热;
D.反应2HI(g)?H2(g)+I2(g)达到平衡后,增大HI的物质的量,容器体积不变,则HI浓度增大,平衡正向移动.
解答 解:A.升高温度,平衡向吸热方向移动,2NO2(g)?N2O4(g),升温时体系颜色加深说明平衡逆向移动,则正反应为放热反应,故A错误;
B.升高温度,氨气浓度降低,氮气和氢气浓度增大,根据化学平衡常数K=$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2}).{c}^{3}({H}_{2})}$知,升高温度平衡常数减小,故B错误;
C.升高温度,平衡向吸热方向移动,CO(g)+H2O(g)?CO2(g)+H2(g),升温时CO的转化率增大,则平衡正向移动,说明正反应为吸热反应,故C正确;
D.反应2HI(g)?H2(g)+I2(g)达到平衡后,增大HI的物质的量,容器体积不变,则HI浓度增大,平衡正向移动,故D错误;
故选C.
点评 本题考查化学平衡移动影响因素,为高频考点,明确温度、浓度对平衡移动影响原理是解本题关键,注意D中压强不影响平衡移动,注意:化学平衡常数只与温度有关,与物质浓度无关.


科目:高中化学 来源: 题型:解答题
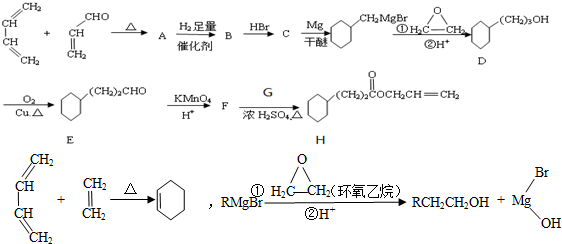
 ,G物质核磁共振氢谱共有4个峰.
,G物质核磁共振氢谱共有4个峰. .写出D生成E的化学方程式
.写出D生成E的化学方程式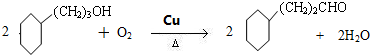 .
.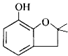 呋喃酚是一种合成农药的重要中间体,它的同分异构体很多,写出符合下列条件的所有芳香族同分异构体的结构简式:
呋喃酚是一种合成农药的重要中间体,它的同分异构体很多,写出符合下列条件的所有芳香族同分异构体的结构简式: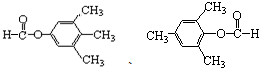 .
.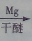 CH3CH2MgBr
CH3CH2MgBr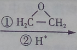 CH3CH2CH2CH2OH.
CH3CH2CH2CH2OH.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
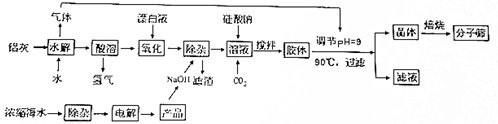
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解过程中阴极和阳极的质量始终保持不变 | |
| B. | 溶液中的Cu2+、H+和Na+都要移向阴极,但在阴极优先放电的离子是Cu2+ | |
| C. | 溶液中的Cl-在阳极上完全放电后,溶液中的SO${\;}_{4}^{2-}$接着在该极上放电生成O2 | |
| D. | 电解过程中阴极上始终有气体产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | V(NO2):V(O2)=2:1 | B. | V(NO):V(O2)=2:1 | ||
| C. | V(NH3):V(O2)=2:1 | D. | V(NO2):V(NO):V(O2)=1:1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 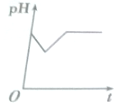 | B. | 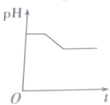 | C. | 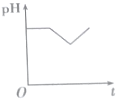 | D. | 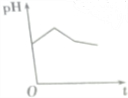 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
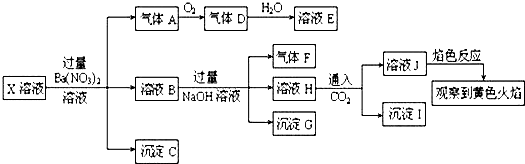
| A. | X中不能确定的离子是Fe3+、A13+、K+、Na+和C1- | |
| B. | 沉淀G中加入盐酸溶解,滴加KSCN溶液显红色,可以确定原溶液中有Fe3+ | |
| C. | 溶液J焰色反应显黄色,则说明原溶液中存在Na+ | |
| D. | 沉淀I一定是A1(OH)3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com