
【题目】现有等物质的量的N2O和CO2 , 下列数值不一定相同的是( )
A.分子数
B.电子数
C.原子数
D.体积
科目:高中化学 来源: 题型:
【题目】现代生产、生活和国防中大量使用电池。如照相机、手机、汽车、卫星等均要使用电池。了解常见电池的工作原理是中学生的必修课之一。请同学们用所学知识回答以下问题。
(1)铅蓄电池放电时的总反应:Pb+PbO2+2H2SO4=2PbSO4+2H2O。请写出放电时正极反应的电极反应式:_________________________。
(2)依据氧化还原反应Zn(s)+Cu2+(aq)===Zn2+(aq)+Cu(s)设计的原电池如图所示。
①请在图中标出电极材料及电解质溶液(写化学式)①___________,②____________,③_______________,④__________________

②盐桥中装有含琼胶的KCl饱和溶液,电池工作过程中盐桥中的Cl-向________极移动(填“左”或“右”)。
(3)燃料电池是一种连续地将燃料和氧化剂的化学能直接转换成电能的化学电池。下图是一个化学过程的示意图。

①A(石墨)电极的名称是_______________。
②通入CH3OH的电极的电极反应式是________________________________。
③乙池中反应的化学方程式为________________________________________。
④当电路中通过0.01mol电子时,丙池溶液的c(H+) = __________mol/L(忽略电解过程中溶液体积的变化)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F、G是前四周期(除稀有气体)原子序数依次增大的七种元素,A的原子核外电子只有一种运动状态;B、C的价电子层中未成对电子数都是2;D、E、F同周期;E核外的s、p能级的电子总数相等;F与E同周期且第一电离能比E小;G的+1价离子(G+)的各层电子全充满。回答问题:
(1)写出E的基态原子的电子排布式___________。
(2)含有元素D的盐的焰色反应为____色,许多金属形成的盐都可以发生焰色反应,其原因是__________________________________________。
(3)由元素A、B、F组成的原子个数比9 : 3 : 1的一种物质,分子中含三个相同的原子团,其结构简式为____________________,该物质遇水爆炸,生成白色沉淀和无色气体,反应的化学方程式为____________________。
(4)G与C可形成化合物GC和G2C,已知GC在加热条件下易转化为G2C,试从原子结构的角度解释发生转化的原因________________________。
(5)G与氮元素形成的某种化合物的晶胞结构如下图所示,则该化合物的化学式为__________,氮原子的配位数为__________。若晶体密度为a g·cm-3,则G原子与氮原子最近的距离为__________pm(写出数学表达式,阿伏加德罗常数的值用NA表示)。
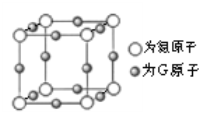
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图表示细胞内某些有机物的元素组成和功能关系,其中A、B代表元素,Ⅰ、Ⅱ、Ⅲ、Ⅳ是生物大分子(多聚体),X、Y、Z、P分别为构成生物大分子的基本单位(单体)。请回答下列问题:
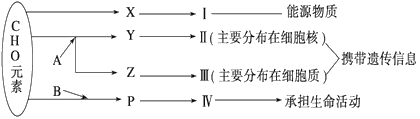
(1)图中X被形容为“生命的燃料”,它是_____,Ⅰ在小麦种子中主要是指________。
(2)A和B各表示_______元素和________元素。
(3)P的结构通式是___________________,组成蛋白质的P的种类约有__________种。
(4)Y和Z在化学组成上的区别是:Z特有的成分是___________(五碳糖)和___________。在观察Z和Y在细胞中的分布时,要用到质量分数为8%的HCl作用为:①________________________________________②__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2013年9月,中国华北华中地区发生了严重的雾霾天气,北京、河北、河南等地的空气污染升为6级空气污染,属于重度污染。汽车尾气、燃煤废气、冬季取暖排放的CO2等都是雾霾形成的原因。
(1)汽车尾气净化的主要原理为:2NO(g)+2CO(g) ![]() N2(g)+2CO2(g) △H<0,在一定温度下,在一体积固定的密闭容器中充入一定量的NO和CO在t1 时刻达到平衡状态。
N2(g)+2CO2(g) △H<0,在一定温度下,在一体积固定的密闭容器中充入一定量的NO和CO在t1 时刻达到平衡状态。
①能判断该反应达到平衡状态的标志是____________________。
A.在单位时间内生成1mol CO2的同时消耗了1mol CO B.混合气体的密度不再改变
C.混合气体的平均相对分子质量不再改变 D.混合气体的压强不再变化
②在t2时刻,将容器的容积迅速扩大到原来的2倍,在其他条件不变的情况下,t3时刻达到新的平衡状态,之后不再改变条件。请在右图中补充画出从t2 到t4 时刻正反应速率随时间的变化曲线:_____________
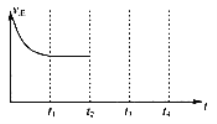
(2)改变煤的利用方式可减少环境污染,通常可将水蒸气通过红热的碳得到水煤气,1.2g 碳完全反应,吸收热量13.13kJ.
①该反应的热化学方程式为______________________________________________
②煤气化过程中产生的有害气体H2S可用足量的Na2C03溶液吸收,该反应的离子方程式为___________________________________________________。(已知:H2S: ![]() ;
; ![]() ;H2CO3:
;H2CO3: ![]() ;
; ![]() )
)
(3)已知反应:CO(g)+H2O(g) ![]() CO2(g)+H2(g),现将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中进行反应,得到如下三组数据:
CO2(g)+H2(g),现将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中进行反应,得到如下三组数据:
实验 | 温度/℃ | 起始量/mol | 平衡量/mol | 达平衡所需时间/min | ||
CO | H2O | H2 | CO | 0 | ||
1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
3 | 900 | a | b | c | d | t |
①实验1条件下平衡常数K=______________(保留小数点后二位)。
②实验3中,若平衡时,CO的转化率大于水蒸气,则a、b必须满足的关系是__________。
③该反应的△H ______0(填“<”或“>”);若在900℃时,另做一组实验,在此容器中加入l0mol CO,5mo1 H2O,2mo1 CO2,5mol H2,则此时v正___________v逆(填“<”,“>”,“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分类法是一种行之有效、简单易行的科学方法。下列关于“Na2CO3”的分类错误的是
A.Na2CO3俗名为纯碱,故它属于碱类B.Na2CO3属于化合物
C.Na2CO3属于强电解质D.Na2CO3属于含氧酸盐
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某可逆反应:mA(g)+nB(g)![]() r C(g)在密闭容器中进行。下图表示此反应在不同时间t,温度T和压强p与反应物B在混合气体中的百分含量(B%)的关系曲线。由曲线分析下列判断正确的是
r C(g)在密闭容器中进行。下图表示此反应在不同时间t,温度T和压强p与反应物B在混合气体中的百分含量(B%)的关系曲线。由曲线分析下列判断正确的是

A. T1>T2,p1>p2,m+n>r,正反应吸热
B. T1<T2,p1<p2,m+n<r,正反应吸热
C. T1>T2,p1>p2,m+n<r,正反应放热
D. T1<T2,p1<p2,m+n>r,正反应放热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】羟氨(NH2OH)是一种还原剂。将16.00mL 0.05mol/L的羟氨酸性溶液与足量硫酸铁在煮沸条件下反应,生成的Fe2+又恰好被24.00mL 0.02mol/L的酸性KMnO4溶液所氧化。在上述反应中,羟氨的氧化产物为( )
A. NO2 B. NO C. N2O D. N2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com