
 ��
��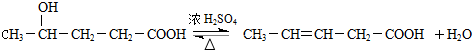 ��
��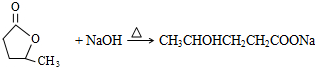 ��
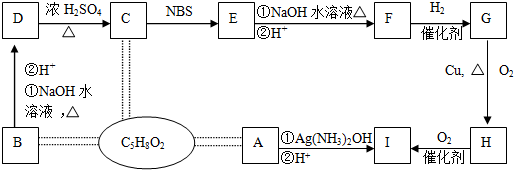
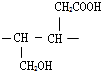
������ �л���A��B��C��Ϊͬ���칹�壬����ʽ��ΪC5H8O2��A��̼����֧������1mol A ����4mol Ag��NH3��2OH��ȫ��Ӧ����ȷ��AΪ���ȩ���ṹ��ʽΪOHC��CH2��3CHO���ɵ�IΪHOOC��CH2��3COOH��B������Ԫ������˵��������4��̼ԭ�Ӻ�1����ԭ�ӣ��һ��ϻ���һ������Bת��ΪD��DΪһ���ǻ��ᣬD�к����ǻ��ܷ�����ȥ��Ӧ����C��C�к���һ��̼̼˫�����Ȼ���C�ܺ�NBS����ȡ����Ӧ�õ�E��E����ˮ�ⷴӦ����F��F�����������ӳɷ�Ӧ����G��G������������������Ӧ����I����I�Ľṹ��֪����E����ԭ�Ӵ���̼��һ�ˣ�������Ŀ�е���֪����֪C�б���CH3-CH=CH-�ṹ�������������C�Ľṹ��ʽΪCH3CH=CHCH2COOH���ɴ˿���ȷ��D���ǻ���λ�ã���D�Ľṹ��ʽΪCH3CH��OH��CH2CH2COOH�������ɵ�B�Ľṹ��ʽΪ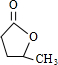 ��EΪCH2Br-CH=CH-CH2COOH��CH2Br-CH=CH-CH2COOH����������ˮ��Һ�����ȷ�Ӧ��������ˮ�⣬���ữ����F����FΪHO-CH2-CH=CH-CH2COOH��F�����������ӳɷ�Ӧ����GΪHOCH2CH2CH2CH2COOH��G����������HΪOHC��CH2��3COOH���ݴ˽��
��EΪCH2Br-CH=CH-CH2COOH��CH2Br-CH=CH-CH2COOH����������ˮ��Һ�����ȷ�Ӧ��������ˮ�⣬���ữ����F����FΪHO-CH2-CH=CH-CH2COOH��F�����������ӳɷ�Ӧ����GΪHOCH2CH2CH2CH2COOH��G����������HΪOHC��CH2��3COOH���ݴ˽��
��� �⣺�л���A��B��C��Ϊͬ���칹�壬����ʽ��ΪC5H8O2��A��̼����֧������1mol A ����4mol Ag��NH3��2OH��ȫ��Ӧ����ȷ��AΪ���ȩ���ṹ��ʽΪOHC��CH2��3CHO���ɵ�IΪHOOC��CH2��3COOH��B������Ԫ������˵��������4��̼ԭ�Ӻ�1����ԭ�ӣ��һ��ϻ���һ������Bת��ΪD��DΪһ���ǻ��ᣬD�к����ǻ��ܷ�����ȥ��Ӧ����C��C�к���һ��̼̼˫�����Ȼ���C�ܺ�NBS����ȡ����Ӧ�õ�E��E����ˮ�ⷴӦ����F��F�����������ӳɷ�Ӧ����G��G������������������Ӧ����I����I�Ľṹ��֪����E����ԭ�Ӵ���̼��һ�ˣ�������Ŀ�е���֪����֪C�б���CH3-CH=CH-�ṹ�������������C�Ľṹ��ʽΪCH3CH=CHCH2COOH���ɴ˿���ȷ��D���ǻ���λ�ã���D�Ľṹ��ʽΪCH3CH��OH��CH2CH2COOH�������ɵ�B�Ľṹ��ʽΪ ��EΪCH2Br-CH=CH-CH2COOH��CH2Br-CH=CH-CH2COOH����������ˮ��Һ�����ȷ�Ӧ��������ˮ�⣬���ữ����F����FΪHO-CH2-CH=CH-CH2COOH��F�����������ӳɷ�Ӧ����GΪHOCH2CH2CH2CH2COOH��G����������HΪOHC��CH2��3COOH��
��EΪCH2Br-CH=CH-CH2COOH��CH2Br-CH=CH-CH2COOH����������ˮ��Һ�����ȷ�Ӧ��������ˮ�⣬���ữ����F����FΪHO-CH2-CH=CH-CH2COOH��F�����������ӳɷ�Ӧ����GΪHOCH2CH2CH2CH2COOH��G����������HΪOHC��CH2��3COOH��
��1��AΪOHC��CH2��3CHO��ϵͳ����Ϊ��1��5-���ȩ���ʴ�Ϊ��1��5-���ȩ��
��2��H�ṹ��ʽΪOHC��CH2��3COOH��F�ļӾ۲�������ڱ�ʾΪ�� ��
��
�ʴ�Ϊ��OHC��CH2��3COOH�� ��
��
��3��EΪCH2Br-CH=CH-CH2COOH��̼̼˫������ԭ�Ӿ�����ͬһƽ���ڣ��Ȼ���̼ԭ�����ӵ�ԭ��Ϊƽ��ṹ��ͨ����ת̼̼����������ʹ2��ƽ�湲�棬һ��E���������5��̼ԭ�ӹ�ƽ�棬
�ʴ�Ϊ��5��
��4��D��C�ķ�Ӧ����ʽ��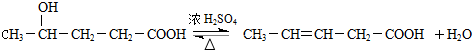 ��
��
B��D��ֻд�������µķ�Ӧ���ķ�Ӧ����ʽ��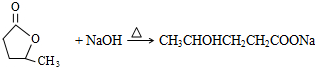 ��
��
�ʴ�Ϊ��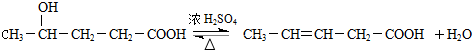 ��
��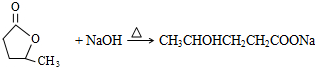 ��
��
��5��G�Ľṹ��ʽΪ��HOOCCH2CH2CH2CH2OH����ͬ���칹����ϣ��پ�����G��ͬ�Ĺ����ţ������ǻ����Ȼ����ں�������������G��ͬ���칹��Ϊ��CH3��2CHCHOHCOOH����CH3��2COHCH2COOH��CH3CHOHCH��CH3��COOH��CH3CH2C��CH3��OHCOOH��HOCH2C��CH3��2COOH����5����
�ʴ�Ϊ��5��
��6����ϩ����NBSȡ������BrCH2CH=CH2��Ȼ������������ˮ��Һ������������ˮ������HOCH2CH=CH2����������ᷢ��������Ӧ����CH3COOCH2CH=CH2���ϳ�·������ͼΪ��CH3CH=CH2$\stackrel{NBS}{��}$BrCH2CH=CH2$��_{��}^{NaOHˮ��Һ}$HOCH2CH=CH2$��_{Ũ����/��}^{CH_{3}COOH}$CH3COOCH2CH=CH2��
�ʴ�Ϊ��CH3CH=CH2$\stackrel{NBS}{��}$BrCH2CH=CH2$��_{��}^{NaOHˮ��Һ}$HOCH2CH=CH2$��_{Ũ����/��}^{CH_{3}COOH}$CH3COOCH2CH=CH2��
���� ���⿼���л��ƶ���ϳɣ��Ƕ��л�������֪ʶ���ۺϿ��飬����A�ķ���ʽ����������Һ��Ӧ������ϵ�ƶ�A�Ľṹ���ۺϷ���ȷ��D���ǻ���λ���ǹؼ������ݷ�Ӧ����������˳�Ʒ������ƶϣ��ܽϺõĿ��鿼������ѧ�����ͷ��������������ѶȽϴ�


 �̲�ȫ���ִʾ�ƪϵ�д�
�̲�ȫ���ִʾ�ƪϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��CCl4��ȡ��ˮ�еĵ� | |
| B�� | ��NaOH��Һ��ȥ�屽�е��� | |
| C�� | �þƾ���ȥ�����еĸ��� | |
| D�� | �ñ���Na2CO3��Һ��ȥ���ᶡ���е����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1molNa2O2�����к���������Ϊ4NA | |
| B�� | ��˫��ˮ�ֽ���ȡ0.1mol������ת�Ƶĵ�������Ϊ0.4��6.02��1023 | |
| C�� | 0.1molAlCl3��ȫˮ��ת��Ϊ�����������壬����0.1NA������ | |
| D�� | VL amol•L-1���Ȼ�����Һ�У���Fe3+����ĿΪ6.02��1023����Cl-����Ŀ����3��6.02��1023 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
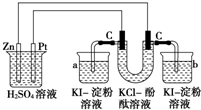 ������ͼ��ͨ��·����Ӧһ��ʱ��ش��������⣨�������ṩ�ĵ��ܿ��Ա�֤��ⷴӦ��˳�����У���
������ͼ��ͨ��·����Ӧһ��ʱ��ش��������⣨�������ṩ�ĵ��ܿ��Ա�֤��ⷴӦ��˳�����У����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��1 mol NH4NO3����ϡ��ˮ��ʹ��Һ�����ԣ���Һ��NH4+��ĿΪNA | |
| B�� | ��״���£�22.4 L�״��к��е�C-H����ĿΪ3NA | |
| C�� | 25��ʱ��pH=2��������Һ�У����е�H+����ĿΪ0.01NA | |
| D�� | 5.6 g Fe��һ����ϡ���ᷴӦ��Fe��ȫ�ܽ�ʱʧȥ�ĵ�����Ϊ3NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | $\frac{b}{��a+b����1{0}^{7}}$ | B�� | $\frac{b}{��a-b����1{0}^{7}}$ | C�� | $\frac{b}{��a-b����1{0}^{5}}$ | D�� | $\frac{a-b}{a��1{0}^{7}}$ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �۵�ϸߣ�Ӳ�Ƚϴ� | B�� | ������ˮ���������л��ܼ� | ||
| C�� | ����ʱ���ܵ��� | D�� | ���Ӽ����ϴ����ܶȽ�С |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
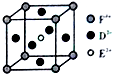 A��B��C��D��E��F��ǰ������ԭ�������������������Ԫ�أ�AԪ��ԭ�ӵĺ����������������Ӳ�����BԪ�ػ�̬ԭ���������ܼ��Ҹ��ܼ���������ͬ��A��D���γ����ֳ���Һ̬������G��H����ԭ����֮�ȷֱ�Ϊ1��1��2��1��EԪ��ԭ�ӵ�K��L�������֮�͵�����M��N�������֮�ͣ�F����Ϊ��������֮��ĵ�������������������ɻ���������������ǡ�����ɴ���������ش����и��⣨�漰Ԫ��������Ӧ��ѧ���ű�ʾ����
A��B��C��D��E��F��ǰ������ԭ�������������������Ԫ�أ�AԪ��ԭ�ӵĺ����������������Ӳ�����BԪ�ػ�̬ԭ���������ܼ��Ҹ��ܼ���������ͬ��A��D���γ����ֳ���Һ̬������G��H����ԭ����֮�ȷֱ�Ϊ1��1��2��1��EԪ��ԭ�ӵ�K��L�������֮�͵�����M��N�������֮�ͣ�F����Ϊ��������֮��ĵ�������������������ɻ���������������ǡ�����ɴ���������ش����и��⣨�漰Ԫ��������Ӧ��ѧ���ű�ʾ����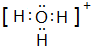 ��
�� �鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com