
| A. | 16O2、18O2互为同位素 | B. | H2O、D2O、T2O的化学性质不同 | ||
| C. | 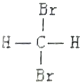 和 和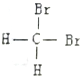 是两种不同结构 是两种不同结构 | D. | 白磷与红磷互为同素异形体 |
分析 A.质子数相同中子数不同的同一元素的不同原子互称同位素,同位素必须原子;
B.同种物质性质相同;
C.由于饱和碳原子是sp3杂化,甲烷是正四面体结构,所以其二溴代物是同一物质;
D.同种元素形成的不同单质互为同素异形体.
解答 解:A.同位素研究的对象是原子,16O2、18O2都是分子,不是原子,故A错误;
B.H2O、D2O、T2O是由H元素的三种同位素原子形成的水,是同种物质,化学性质相同,故B错误;
C.由于饱和碳原子是sp3杂化,甲烷是正四面体结构,所以其二溴代物是同一物质,结构相同,故C错误;
D.同种元素形成的不同单质,互为同素异形体;故D正确.
故选D.
点评 本题考查化学“五同”比较,题目难度不大,注意把握概念的内涵与外延.


科目:高中化学 来源: 题型:选择题
| A. | 将Cu片置于浓H2SO4中,无明显现象,说明Cu在冷的浓硫酸中被钝化 | |
| B. | SO2具有漂白性所以它能使碘的淀粉溶液由蓝色变为无色 | |
| C. | 向装有Fe(NO3)2溶液的试管中加入稀H2SO4,在管口观察到红棕色气体 | |
| D. | SO2和Cl2分别与双氧水反应均产生O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 热稀盐酸 | B. | 热浓盐酸 | C. | 热烧碱溶液 | D. | 热水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2SO4与Ba(OH)2溶液反应:Ba2++2OH-+2H+十SO42-→BaSO4↓+2H2O | |
| B. | CuSO4溶液与NaOH溶液反应:Cu2++2OH-→Cu(OH)2↓ | |
| C. | NaOH溶液中通入少量CO2:2OH-+CO2→CO32-+H2O | |
| D. | CH3COOH溶液与NaOH溶液反应:H++OH-→H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | $\frac{1}{2}$H2SO4(aq)+$\frac{1}{2}$Ba(OH)2(aq)═$\frac{1}{2}$BaSO4(s)+H2O(l) | |
| B. | 2KOH(aq)+H2SO4(aq)═K2SO4(aq)+2H2O(l) | |
| C. | CH3COOH(aq)+NaOH(aq)═CH3COONa(aq)+H2O(l) | |
| D. | NH3•H2O(aq)+HCl(aq)═NH4Cl(aq)+H2O(l) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
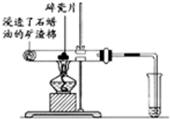 (1)写出下列反应的化学方程式:
(1)写出下列反应的化学方程式: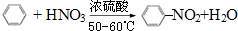 .
.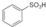 ),根据质量守恒定律,可判断出另一个反应产物为H2O.
),根据质量守恒定律,可判断出另一个反应产物为H2O.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com