
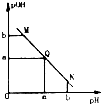
 某温度下,向一定体积0.1mol/L醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中pOH(pOH=-1g[OH+])与pH的变化关系如图所示,则
某温度下,向一定体积0.1mol/L醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中pOH(pOH=-1g[OH+])与pH的变化关系如图所示,则分析 酸溶液中pOH越大,说明溶液中氢氧根离子浓度越小,溶液氢离子浓度越大,酸性越强,随着NaOH的加入,发生中和反应,溶液氢氧根离子的浓度逐渐增大,则溶液pOH逐渐减小,pH逐渐增大,结合弱电解质的电离解答该题.
解答 解:(1)由于醋酸是弱酸,电离程度很小,离子浓度也较小,M点溶液的导电能力最弱,故答案为:弱;
(2)N点所示溶液为碱性,根据溶液电荷守恒易判断出此时c(Na+)>c(CH3COO-),故答案为:<;
(3)由于M点的H+浓度等于N点的OH-浓度,对水的电离程度抑制能力相同,所以两点水电离程度相同,故答案为:=;
(4)Q点的pOH=pH,溶液为中性,而两者等体积混合后生成醋酸钠,水解显碱性.则所加NaOH溶液体积略小于醋酸溶液的体积,故答案为:<.
点评 本题考查酸碱中和的定性判断和计算,侧重于弱电解质的电离的考查,注意弱电解质的电离特点,把握pOH的含义,题目难度中等.


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 用食醋除去暖瓶内的水垢 | B. | 鸡蛋白溶液遇硝酸变黄 | ||
| C. | 碘单质遇淀粉变蓝 | D. | 用汽油洗去衣物上的油污 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子晶体、离子晶体、分子晶体、金属晶体中都一定存在化学键 | |
| B. | 氧化物不可能是还原产物,只可能是氧化产物 | |
| C. | 原子晶体熔点不一定比金属晶体高,分子晶体熔点不一定比金属晶体低 | |
| D. | 固态导电的一定是金属晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硝酸钾和金刚石 | B. | 晶体硅和水晶 | C. | 冰和干冰 | D. | 氯化钠和蔗糖 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 变化过程中化学键被破坏,则一定发生化学变化 | |
| B. | 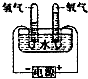 实验室制氧气 | |
| C. | Na+、Fe3+-人体所需微量元素 | |
| D. | 能区别地沟油与矿物油的方法是加入足量氢氧化钠溶液共热,不分层的是地沟油 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 9种 | B. | 10种 | C. | 13种 | D. | 17种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 它是一种含氮的有机化合物 | |
| B. | 它的相对分子质量为126g/mol | |
| C. | 它易溶于苯、四氯化碳等有机溶剂 | |
| D. | 由于它的含氮量高,被不法商人添加到奶粉中,以提升奶粉检测中的蛋白质含量指标 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
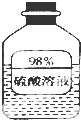 (1)如图信息,瓶中溶液长期放置后溶质质量分数变小,是因为该物质具有吸水性.
(1)如图信息,瓶中溶液长期放置后溶质质量分数变小,是因为该物质具有吸水性.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 中学化学中几种常见物质的转化关系如图所示,且已知将F的饱和溶液滴入沸水中,煮沸可得到以H为分散质的红褐色胶体.请回答下列问题:
中学化学中几种常见物质的转化关系如图所示,且已知将F的饱和溶液滴入沸水中,煮沸可得到以H为分散质的红褐色胶体.请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com