
| A. | 通入CH4的电极为正极 | |
| B. | 通入CH4的电极反应为:CH4+10OH-→CO32-+7H2O+8e- | |
| C. | 通入O2的电极为负极 | |
| D. | 放电时溶液中阴离子向正极移动 |
分析 该燃料电池中,通入甲烷的电极是负极、通入氧气的电极是正极,电解质溶液呈碱性,通入CH4的电极电极反应式为CH4+10OH--8e-=CO32-+7H2O,通入氧气的电极反应式为O2+2H2O+4e-=4OH-;放电时电解质溶液中阴离子向负极移动、阳离子向正极移动,据此分析解答.
解答 解:A.燃料电池中,通入燃料的电极上失电子发生氧化反应,所以通入燃料的电极是负极,则通入甲烷的电极是负极,故A错误;
B.通入甲烷的电极上失电子和氢氧根离子反应生成碳酸根离子和水,电极反应式为CH4+10OH-→CO32-+7H2O+8e-,故B正确;
C.燃料电池中,通入氧气的电极上得电子发生还原反应,所以通入氧气的电极是正极,故C错误;
D.放电时,负极附近聚集大量阳离子,所以电解质溶液中阴离子向负极移动,正极上聚集大量电子,电解质溶液中阳离子向正极移动,故D错误;
故选B.
点评 本题考查化学电源新型电池,为高频考点,明确各个电极上发生的反应是解本题关键,难点是电极反应式的书写,易错选项是D.


科目:高中化学 来源:2017届河南省高三上第一次联考化学试卷(解析版) 题型:选择题
下列设计的实验 方案能达到实验目的的是()
方案能达到实验目的的是()
A.制备Al(OH)3悬浊液:向lmol.L-1的AlCl3溶液中加过量的6mol.L-1NaOH溶液
B.提纯含有少量乙酸的乙酸乙酯:向含有少量乙酸的乙酸乙酯中加入氢氧化钠溶液,振荡后静置分液,并除去有机相的水
C.检验溶液中是否含有Fe3+:取少量待检验溶液,向其中加入少量新制氯水,再滴加KSCN溶液,观察实验现象
D.探究催化剂对H2O2分解速率的影响:在 相同条件下,向一支试管中加入2ml5%H2O2和1mlH2O,向另一支试管中加入2mL5%H2O2和1mLFeCl3溶液,观察并比较实验现象
相同条件下,向一支试管中加入2ml5%H2O2和1mlH2O,向另一支试管中加入2mL5%H2O2和1mLFeCl3溶液,观察并比较实验现象
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓NaOH溶液 | B. | 饱和食盐水 | C. | 石灰乳 | D. | 浓硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 干水是纯净物 | B. | 干水和干冰是同一种物质 | ||
| C. | 干水中的水分子不再运动 | D. | 用干水能更好地吸收CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5.6gFe和足量的盐酸完全反应失去电子数为0.3 NA | |
| B. | 1.0mol•L的NaCl 溶液中Na+数为NA | |
| C. | 16gCH4所含的电子数为10NA | |
| D. | 标况下,4.48L的水中含有H2O分子的数目为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C2H2 | B. | C2H4 | C. | C3H4 | D. | C6H6 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
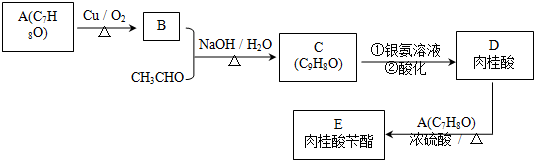

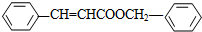 .
. .
. .
.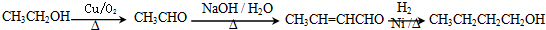 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com