
����Ŀ��Ԫ��A��B��C��D��E��F��G��Ԫ�����ڱ��е�λ����ͼ1��ʾ���ش��������⣺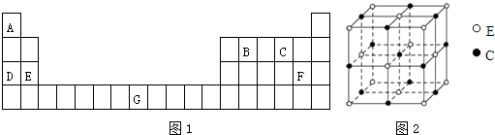
��1��G�Ļ�̬ԭ�Ӻ�������Ų�ʽΪ �� ԭ�ӵĵ�һ�����ܣ�DE���������������
��2�����ݼ۲���ӻ������ۣ��۲���Ӷ�֮��ij�����С������˳��l��l��l��b��b��b��lΪ�¶Ե��Ӷԣ�bΪ���ϵ��Ӷԣ��������A2C�е�A��C��A���ǿɵó��Ľ����� ��
A.180��
B.�ӽ�120�㣬��С��120��
C.�ӽ�120�㣬������120��
D.�ӽ�109��28�䣬��С��109��28��
��3��������G��BC��5���۵�Ϊ��20�棬�е�Ϊ103�棬������������壬�������д��ڵĻ�ѧ�������� �� ���ڿ�����ȼ�����ɺ���ɫ�������Ӧ�Ļ�ѧ����ʽΪ ��
��4��������BCF2�����幹��Ϊ �� ����Bԭ�ӵ��ӻ���������� �� д��������BCF2������ͬ�ռ乹�͵ĺ���������� ��
��5��������EC�ľ����ṹ��ͼ2��ʾ����������a=0.424nm��ÿ�������к�����E2+ �� ��ʽ����EC������ܶ� gcm��3 ��
���𰸡�
��1��1s22s22p63s23p63d64s2����
��2��D
��3�����ӣ���λ�������ۼ���4Fe��CO��3+9O2 ![]() 2Fe2O3+12CO2
2Fe2O3+12CO2
��4��ƽ�������Σ�sp2��NO3����CO32����
��5��4��3.49
���������⣺��Ԫ�������ڱ��е�λ�ã���֪AΪHԪ�ء�BΪ̼Ԫ�ء�CΪOԪ�ء�DΪNaԪ�ء�EΪMg��FΪCl��GΪFe����1��Feԭ�Ӻ��������Ϊ26����Fe�Ļ�̬�����Ų�ʽΪ1s22s22p63s23p63d64s2 �� ������Na��Mg��Mg��3s����Ϊȫ���ȶ��ṹ����ԭ�ӵĵ�һ�����ܣ�D��E��
���Դ��ǣ�1s22s22p63s23p63d64s2��������2��H2O�к�2�Թ¶Ե��ӣ�2�����ϵ��Ӷԣ�ΪV�ͽṹ�����ǽӽ�109��28�䣬��С��109��28�䣬��ѡD����3��������Fe��CO��3���۵�Ϊ��20�棬�е�Ϊ103�棬�۷е�Ƚϵͣ����ڷ��Ӿ��壬����λ�������ۼ������ڿ�����ȼ�����ɺ���ɫ�������������Ϊ�������������ɶ�����̼����Ӧ����ʽΪ��4Fe��CO��3+9O2 ![]() 2Fe2O3+12CO2 ��
2Fe2O3+12CO2 ��
���Դ��ǣ����ӣ���λ�������ۼ���4Fe��CO��3+9O2 ![]() 2Fe2O3+12CO2����4��������COCl2��Cԭ���γ�3���Ҽ���û�й¶Ե��ӣ��۲���Ӷ���Ϊ3��Cԭ��Ϊsp2�ӻ����ռ�ṹΪƽ�������Σ���COCl2������ͬ�ռ乹�͵ĺ���������ӵ�����ԭ������3��Oԭ����û�й¶Ե��ӣ�ΪNO3����CO32���ȣ�
2Fe2O3+12CO2����4��������COCl2��Cԭ���γ�3���Ҽ���û�й¶Ե��ӣ��۲���Ӷ���Ϊ3��Cԭ��Ϊsp2�ӻ����ռ�ṹΪƽ�������Σ���COCl2������ͬ�ռ乹�͵ĺ���������ӵ�����ԭ������3��Oԭ����û�й¶Ե��ӣ�ΪNO3����CO32���ȣ�
���Դ��ǣ�ƽ�������Σ�sp2��NO3����CO32���ȣ���4��������Mgԭ����ĿΪ6�� ![]() +8��
+8�� ![]() =4��Oԭ����Ŀ=1+12��
=4��Oԭ����Ŀ=1+12�� ![]() =4��������Ϊ4��
=4��������Ϊ4�� ![]() g���������������߳���Ϊ0.424nm������٤������ΪNA �� �þ�����ܶ�Ϊ 4��
g���������������߳���Ϊ0.424nm������٤������ΪNA �� �þ�����ܶ�Ϊ 4�� ![]() g�£�0.424��10��7cm��3=3.49 g��cm��3 ��
g�£�0.424��10��7cm��3=3.49 g��cm��3 ��
���Դ��ǣ�4��3.49��


 ��ĩ���100�ִ��½����ȫ�Ծ�ϵ�д�
��ĩ���100�ִ��½����ȫ�Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ȼ�ѧ����ʽ��д��ȷ���ǣ���H�ľ���ֵ����ȷ���� ��
A.C��s��+ ![]() O2��g���TCO��g����H=��110.5KJmol��1��ȼ���ȣ�
O2��g���TCO��g����H=��110.5KJmol��1��ȼ���ȣ�
B.C2H5OH+3O2�T2CO2+3H2O��H=��1368.8KJmol��1����Ӧ�ȣ�
C.2NaOH��aq��+H2SO4��aq���TNa2SO4��aq��+2H2O ��l����H=��114.6KJmol��1���к��ȣ�
D.2H2O��g���T2H2��g��+O2��g����H=+483.6KJmol��1����Ӧ�ȣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҩ�����ʶ��ʹ����ȷ����
A. ��ðʱ����������˾ƥ��B. ��ҩ��û�и�����
C. �������������˿�����D. θ�����ֻҪ��������������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧС��Ϊ��֤��SO2��Cl2��Ư���ԣ��������ͼ��ʾ��ʵ��װ����

��1��ʵ�����Ʊ�Cl2�����ӷ���ʽ��_____________________________��Ӧѡ����ͼA��Eװ���е�______������ţ���Cl2����Ӧ��Ũ���������ֳ���������_________________��
��2����Ӧ��ʼ����B��D�����Թ��е�Ʒ����Һ����ɫ��ֹͣͨ����B��D�����Թ��е�Һ����ȣ�B�Թ��е�������___________________________________��
��3��װ��C��������____________________________________��
��4����������ͬѧ�ֱ�������ͼ��ʾװ��̽���������尴��ͬ������Ϻ��Ư���ԡ��Է�����

�����������Ʒ����Һ֮ǰ���Ƚ�SO2��Cl2ͨ��ʢ��Ũ����װ�õ�Ŀ����_____________________��
����ͬѧ��ʵ������з�����ͨ��һ��ʱ���Ʒ����Һ��������ɫ����ԭ����������Ӧ�����ӷ���ʽ������____________
����ͬѧ��ʵ������з�����ͨ��һ��ʱ���Ʒ����Һ��ɫ��ʱ�����Ʊ��Խ��Խdz��ԭ����_______________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʳ���ʱ����ɫ��ȷ����
A. CaCO3 �� ����ɫB. BaSO4 ������ɫC. Al(OH)3 �� ��ɫD. AgCl �� ��ɫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����KCl��MgCl2��Mg��NO3��2�γɵĻ����Һ�У�c��K+��=0.1mol/L��c��Mg2+��=0.15mol/L��c��Cl����=0.2mol/L����c��NO3����Ϊ�� ��
A.0.05 mol/L
B.0.20 mol/L
C.0.30 mol/L
D.0.40 mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������Һ�������ͺ��Ȼ�����Һ ��39�����Ҵ���Һ �������ƺ͵������ˮ�� Һ���������ϸ����Һ����ȷ���������� ( )
A. ��Һ����ȡ������ B. ��Һ��������ȡ
C. ��ȡ������Һ D. ������ȡ����Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڷ�Ӧ��4CO��g��+2NO2��g��=4CO2��g��+N2��g����H=��1200kJmol��1 �� �¶Ȳ�ͬ ��T2��T1������������ͬʱ������ͼ����ȷ���ǣ� ��
A.
B.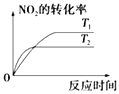
C.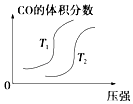
D.
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com