

| 选项 | 甲 | 乙 | 丙 | 试管中现象 |
| A | 浓氨水 | 生石灰 | Al(SO4)3溶液 | 先沉淀后消失 |
| B | 浓硝酸 | 铜 | 淀粉KI溶液 | 试管口出现红棕色溶液仍为无色 |
| C | 浓盐酸 | 二氧化锰 | 石蕊溶液 | 先变红后褪色 |
| D | 双氧水 | 二氧化锰 | 氢硫酸 | 溶液出现浑浊 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.Al(OH)3易溶于强碱但难溶于弱碱溶液;
B.二氧化氮呈红棕色且具有氧化性,能氧化碘离子生成碘单质,碘遇淀粉试液变蓝色;
C.二氧化锰和浓盐酸制取氯气需要加热;
D.氧气具有氧化性,能氧化氢硫酸生成S单质.
解答 解:A.浓氨水和生石灰混合,CaO和水反应放出的热量导致一水合氨分解生成氨气,氨气极易溶于水生成一水合氨,一水合氨能Al(SO4)3发生复分解反应,Al(OH)3易溶于强碱但难溶于弱碱氨水溶液,所以试管中生成白色沉淀但沉淀不溶解,故A错误;
B.铜和浓硝酸反应生成红棕色气体二氧化氮,二氧化氮具有强氧化性,能和碘离子反应生成碘单质,碘遇淀粉试液变蓝色,所以丙中溶液呈蓝色,故B错误;
C.二氧化锰和浓盐酸制取氯气需要加热,该实验没有加热,所以没有氯气生成,故C错误;
D.氧气具有氧化性,能氧化氢硫酸生成S单质,所以丙中产生淡黄色沉淀,溶液出现浑浊,故D正确;
故选D.
点评 本题考查化学实验方案评价,为高频考点,涉及气体制取、氧化还原反应、物质性质等知识点,明确实验原理及物质性质是解本题关键,注意氢氧化铝的两性及二氧化氮的强氧化性,易错选项是B.


 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:选择题
| A. | 2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑ | B. | Fe+CuSO4═FeSO4+Cu | ||
| C. | 2H2O $\frac{\underline{\;通电\;}}{\;}$ 2H2↑+O2↑ | D. | Cl2+2NaOH═NaCl+NaClO+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 14 | B. | 28 | C. | 31 | D. | 35.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
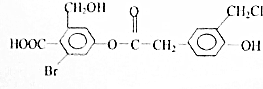 有机物N的结构如图所示,1mol有机物N在一定条件下分别与足量NaOH(溶液),NaHCO3(溶液),H2反应理论上消耗这3种物质的物质的量之比为( )
有机物N的结构如图所示,1mol有机物N在一定条件下分别与足量NaOH(溶液),NaHCO3(溶液),H2反应理论上消耗这3种物质的物质的量之比为( )| A. | 8:1:7 | B. | 5:1:6 | C. | 5:2:6 | D. | 7:1:6 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
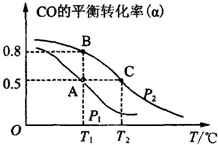 (1)已知:3H2(g)+3CO(g)═CH3OCH3(g)+CO2(g),△H=-247kJ/mol.一定条件下的密闭容器中,该总反应达到平衡,要提高CO的转化率,可以采取的措施是AE.
(1)已知:3H2(g)+3CO(g)═CH3OCH3(g)+CO2(g),△H=-247kJ/mol.一定条件下的密闭容器中,该总反应达到平衡,要提高CO的转化率,可以采取的措施是AE.| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度/(mol•L-1) | 0.01 | 0.2 | 0.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图所示装置可用来制取和观察Fe(OH)2在空气中被氧化时颜色的变化.实验时必须使用铁屑和6mol/L的硫酸,其他试剂任选.填写下列空白.
如图所示装置可用来制取和观察Fe(OH)2在空气中被氧化时颜色的变化.实验时必须使用铁屑和6mol/L的硫酸,其他试剂任选.填写下列空白.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com