
| A. | 氯化钠 | B. | 氯化钾 | C. | 氯化铜 | D. | 氯化铝 |
分析 假设5.55g全部为CaCl2,则生成AgCl为$\frac{5.55g}{111g/mol}$×2×143.5g/mol=14.35g<15g,故除杂氯化物中氯元素含量应大于CaCl2中氯元素含量,若全部为杂质,生成AgCl的质量应大于15g.
解答 解:假设5.55g全部为CaCl2,则生成AgCl为$\frac{5.55g}{111g/mol}$×2×143.5g/mol=14.35g<15g,故除杂氯化物中氯元素含量应大于CaCl2中氯元素含量,若全部为杂质,生成AgCl的质量应大于15g.
CaCl2中Ca、Cl质量之比为40:71,而NaCl中Na、Cl质量之比为46:71,KCl中K、Cl质量之比为78:71,CuCl2中Cu、Cl质量之比为64:71,AlCl3中Al、Cl质量之比为27:35.5×3=18:71,故AlCl3中氯元素含量大于CaCl2中氯元素含量,
假设5.55g全部为AlCl3,生成AgCl沉淀为$\frac{5.55g}{133.5g/mol}$×3×143.5g/mol≈17.9g>15g,符合题意,
故选:D.
点评 本题考查混合物的计算,题目难度中等,注意用端值法解答,属于易错题目,学生容易考虑氯元素含量大于氯化钙中氯元素含量,忽略若全部为杂质时生成AgCl的质量应大于15g.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | ③⑤ | B. | ②③ | C. | ②④ | D. | ①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 150ml 1mol/L氯化钠溶液 | B. | 150ml 3mol/L氯化钾溶液 | ||
| C. | 75ml 2mol/L氯化铵溶液 | D. | 50ml 1mol/L氯化钡溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
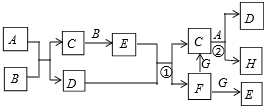 下列有关物质的转化关系如图所示(部分物质与条件已略去,其中反应②的条件是“700℃,催化剂”).G是常见的红色金属单质,B、H是空气的主要成分,A、C、E均是常见气体,D是最常见的无色液体.请回答下列问题:
下列有关物质的转化关系如图所示(部分物质与条件已略去,其中反应②的条件是“700℃,催化剂”).G是常见的红色金属单质,B、H是空气的主要成分,A、C、E均是常见气体,D是最常见的无色液体.请回答下列问题: .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
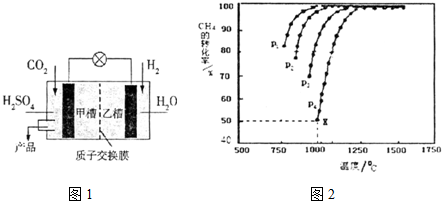 第21届联合国气候大会于2015年11月30日在巴黎召开,会议的主题是减 少温室气体排放量.
第21届联合国气候大会于2015年11月30日在巴黎召开,会议的主题是减 少温室气体排放量.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素代号 | I1 | I2 | I3 | I4 |
| Q | 2080 | 4000 | 6100 | 9400 |
| R | 500 | 4600 | 6900 | 9500 |
| S | 740 | 1500 | 7700 | 10500 |
| T | 580 | 1800 | 2700 | 11600 |
| U | 420 | 3100 | 4400 | 5900 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Al14和稀盐酸反应的化学方程式可表示为Al14+2HCl→Al14Cl2+H2↑ | |
| B. | Al13超原子中Al原子间是通过共价键结合的 | |
| C. | Al14、Al13性质与Al相似,都具有较强的还原性 | |
| D. | Al13和Al14互为同位素 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com