B
分析:A.过氧化钠既是氧化剂又是还原剂,过氧根离子中的氧为-1价,一半氧原子化合价升高,生成氧气,另一半氧原子化合价降低,生成-2价的氧;
B.乙醛、乙酸乙酯的含碳量相同;
C.CH
3COOH抑制水的电离,根据K
W=c(H
+)?c(OH
-)=1×10
-14解题;
D.标准状况下,三氯甲烷是液体.
解答:A.过氧化钠既是氧化剂又是还原剂,过氧根离子中的氧为-1价,一半氧原子化合价升高,生成氧气,另一半氧原子化合价降低,生成-2价的氧,故1mol过氧化钠参与反应时转移电子的量为1 mol,7.8gNa
2O
2的物质的量是0.1mol,转移电子数为0.1N
A,故A错误;
B.乙醛、乙酸乙酯的最简式都是C
2H
4O,4.4g×
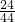
=2.4g,即碳原子的物质的量是0.2mol,含碳原子数为0.2N
A,故B正确;
C.HCOOH溶液中的氢离子一部分是由醋酸和水两者共同电离,但其中氢氧根离子全由水电离,可以根据K
W=c(H
+)?c(OH
-)=1×10
-14这个关系算出水电离的氢离子的浓度为
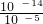
=10
-9,故C错误;
D.标准状况下,三氯甲烷是液体,2.24L三氯甲烷的物质的量不是0.1mol,故D错误.
故选B.
点评:本题考查阿伏加德罗常数,题目难度不大,注意物质的组成、结构、性质以及物质存在的外界条件和聚集状态等问题.

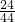 =2.4g,即碳原子的物质的量是0.2mol,含碳原子数为0.2NA,故B正确;
=2.4g,即碳原子的物质的量是0.2mol,含碳原子数为0.2NA,故B正确;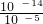 =10-9,故C错误;
=10-9,故C错误;

 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案