
| A.Zn(s)+CuSO4(aq)===ZnSO4(aq)+Cu(s) ΔH=-216 kJ·mol-1,E反应物<E生成物 |
| B.CaCO3(s)===CaO(s)+CO2(g) ΔH=+178.5 kJ·mol-1,E反应物<E生成物 |
| C.HI(g)??H2(g)+I2(s) ΔH=-26.5 kJ·mol-1,1 mol HI在密闭容器中分解达平衡后放出26.5 kJ的能量 |
| D.H+(aq)+OH-(aq)===H2O(l) ΔH=-57.3 kJ·mol-1,1 L 1 mol·L-1的NaOH溶液与含0.5 mol H2SO4的浓硫酸混合后放热57.3 kJ |
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案科目:高中化学 来源:不详 题型:填空题
 (g) △H=-25 KJ/mol
(g) △H=-25 KJ/mol 
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
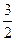 C(s)=
C(s)=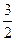 CO2(g)+2Fe(s) △H= +234.1kJ·mol-1 C(s) + O2(g) = CO2(g) △H=-39
CO2(g)+2Fe(s) △H= +234.1kJ·mol-1 C(s) + O2(g) = CO2(g) △H=-39 3.5kJ·mol-1 则2Fe(s)+
3.5kJ·mol-1 则2Fe(s)+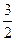 O2(g)= Fe2O3(s)的△H是
O2(g)= Fe2O3(s)的△H是
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 密闭容器中,充入1 mol CO2和3 mol H2,一定条件下发生反应:CO2(g)+3H2(g)
密闭容器中,充入1 mol CO2和3 mol H2,一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH=-49.0kJ/mol
CH3OH(g)+H2O(g) ΔH=-49.0kJ/mol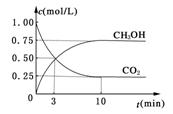
 n)。
n)。 ΔH=-1277 kJ·mol-1
ΔH=-1277 kJ·mol-1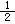 O2(g)=CO(g) ΔH=-110.5 kJ·mol-1
O2(g)=CO(g) ΔH=-110.5 kJ·mol-1 ,中国科学院长春应用化学研究所在甲醇燃料电池技术方面获得新突破,组装出了自呼吸电池及主动式电堆。甲醇燃料电池的工作原理如下图所示。
,中国科学院长春应用化学研究所在甲醇燃料电池技术方面获得新突破,组装出了自呼吸电池及主动式电堆。甲醇燃料电池的工作原理如下图所示。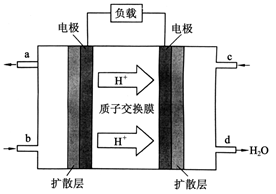

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 。
。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 。
。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com