
����Ŀ��ij��ѧ��ȤС��ⶨ��������Ҫ�ɷ�FeS2����������Ԫ�ص�������������������ʵ�飺��m1g��Ʒ������ͼ��ʾװ��C�У���K1�ر�K2����a������ͨ���������������ʯӢ���е���Ʒ��

��ش��������⣺
��1��װ��B������Ϊ_____��a������ͨ�������Ŀ����_____��
��2��װ��A��������_____��
��3����Ӧ�����ر�K1��K2������ƿ�м���Һ�壬��ȼG���ƾ��ƣ�ʹ��ƿ�з�Ӧ����������������ͼ��

�ٲ���I������Һ��������������_____��
�ڲ�������ϴ�ӡ���ɡ����أ���������Ƿ�ϴ���ķ�����_____��
�۸�����������Ԫ�ص���������Ϊ_____���ú�m1��m2�Ĵ���ʽ��ʾ��
��4��ȡ���պ������������Fe2O3��FeO��������֤���д���FeO��Ӧѡ�õ��Լ���_____��
���𰸡����θ���� �ṩ����ʹ��������ȼ�գ�ͬʱʹ�������ɵĶ�������������ȫ��D������������Һ���� ����ͨ���������ʹ֮ƽ�� Na2SO4��NaCl��NaClO ȡ���һ��ϴ��Һ�������Թ��е������������ữ����������Һ�����ޱ�ʯ�������������Ѿ�ϴ�� ![]() ��100% ϡ���ᡢ���������Һ
��100% ϡ���ᡢ���������Һ
��������
��1�����������Ľṹ��֪��װ��B������Ϊ���θ���ܣ�a������ͨ�������Ŀ�����ṩ����ʹ��������ȼ�գ�ͬʱʹ�������ɵĶ�������������ȫ��D������������Һ���գ�
��2��װ��A�������ǿ���ͨ���������ʹ֮ƽ�ȣ�
��3����D�ж����������������������Һ��Ӧ��������������Һ��Dƿ��Ϊ�������ƺ��������ƵĻ����Һ��ͨ���������������������������������������������ƺ����ᣬ�������������Ʒ�Ӧ�����Ȼ��ƺ�ˮ�������������������Ʒ�Ӧ�����Ȼ��ƺʹ������ƣ��ʲ���I������Һ��������������Na2SO4��NaCl��NaClO��
�ڲ�������ϴ�ӡ���ɡ����أ���������Ƿ�ϴ���ķ�����ȡ���һ��ϴ��Һ�������Թ��е������������ữ����������Һ�����ޱ�ʯ�������������Ѿ�ϴ����
�۲������õ�m2g����Ϊ���ᱵ������������ԭ���غ㣬������������Ԫ�ص�����Ϊ![]() g��������������Ԫ�ص���������Ϊ
g��������������Ԫ�ص���������Ϊ![]() ��100%��
��100%��
��4��ȡ���պ������������Fe2O3��FeO��������֤���д���FeO������+3����������¼���+2����Ӧ����+2�����Ļ�ԭ�Խ��м��飬��ѡ�õ��Լ���ϡ���ᡢ���������Һ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�������Լ�ƿ��ǩ�ϵ����ݣ�

(1)ij��ѧ��ȤС������������ʵ�ʵ��̽��ʱ����Ҫ490mL 4.6mol��L-1��ϡ���ᣬ��Ҫ���Ƹ�Ũ�ȵ���Һ����IJ�����������Ͳ���ձ�������������ͷ�ι��⣬����Ҫ__________(����������)����Ҫ��ȡ98%Ũ����____________mL�������ƣ�
(2)������Һʱ�����²�����a.ϡ���ܽ�b.ҡ��c.ϴ��d.��ȴe.��ȡf.����Һ��������ƿg.���ݣ�ʵ�����˳����ȷ������___________����
A. e��a��f��d��c��f��g��b B. e��a��d��f��c��f��g��b
C. e��a��f��d��c��f��b��g D. e��a��d��f��c��f��b��g
(3)����Ϊ���ƹ����в��ֲ�����ʾ��ͼ�������д������____(�����)��

(4)������4.6mol��L-1ϡ����Ĺ����У���������������������õ�������Һ���ʵ���Ũ��ƫ�ߵ���___��
A.δ����ȴ���Ƚ���Һע������ƿ�� B.����ƿϴ�Ӻ�δ���ﴦ��
C.����ʱ���ӹ۲�Һ�� D.δϴ���ձ��Ͳ�����
(5)Ϊ�к�100mL 2.3 mol��L-1KOH��Һ�������ԣ���Ҫ����________mL 4.6mol��L-1ϡ���ᡣ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ���ǣ� ��
A.�ƺͼصĺϽ�����ڿ����ӷ�Ӧ�����Ƚ�����
B.ʵ���ҳ����Ʊ�����ú�ͻ����Ȼ�̼��
C.С�մ������Ƹ�����õķ��ͷ۵���Ҫ�ɷ�֮һ
D.�ȵĴ�����Һ����ȥ����Ʒ���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D���ֶ�����Ԫ�أ�ԭ������D>C>B>A����B��C��Dͬ���ڣ�A��Dͬ���壬Bԭ�ӵ������ֻ��һ�����ӣ�C��ԭ�ӽṹʾ��ͼ��ͼ��D��ͬ����Ԫ����ԭ�Ӱ뾶��С���ݴ���գ�
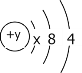
��1��CԪ�ص�����Ϊ____������̬�⻯��Ļ�ѧʽΪ___��
��2��D�����ڱ���___���ڣ�___�塣
��3��A��B��C��D����Ԫ�ص�ԭ�Ӱ뾶�ɴ�С��˳��Ϊ���û�ѧʽ��д��___
��4��B������������ˮ����Ļ�ѧʽΪ__
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л��������ۼ���ϩ��������������ʸߡ������ᡢ��ȫ���ܸߵ��ŵ㣬Ŀǰ���㷺�������������DZ�������������֡���ѧ��Ƭ�����ݶ����绰ͤ�������䡢��־�Ƶȡ�
��ͼ����2������ϩΪԭ�Ϻϳ��л�����E������2������ϩ���������·�ߣ�

(1)�л������� �к��еĹ�����������_____________________________________��
�к��еĹ�����������_____________________________________��
(2)д��B�Ľṹ��ʽ��___________________________________
(3)д����Ӧ�ٵĻ�ѧ����ʽ____________________________________________________________________
(4)д����Ӧ�Ļ�ѧ����ʽ__________________________________________________________________
(5)�������� ~ ��Ӧ�У�����ȡ����Ӧ����______________�����ڼӳɷ�Ӧ����___________��
(6)д��E�Ľṹ��ʽ��___________________________
(7)д���л��� ͨ�������γɸ߷��Ӿ���F�Ľṹ��ʽ��___________________________
ͨ�������γɸ߷��Ӿ���F�Ľṹ��ʽ��___________________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�����ú�̼���⡢������Ԫ�ص��л���A��BΪԭ�Ϻϳ��л�������H��C11H12O2����·��ʾ��ͼ���£�

��֪: ����ȩ���Ӽ��ܷ������·�Ӧ��
 ����R����R����ʾ��ԭ�ӻ�������
����R����R����ʾ��ԭ�ӻ�������
(1)�������ⶨ���л���A����Է�������Ϊ46����Ԫ�ط���֪A������C��H��Oԭ�Ӹ�����Ϊ2:6:1 �����л���A�ķ���ʽΪ______________
(2)�����廯����B�ķ���ʽΪC7H8O��C�����Ʒ�Ӧ��������NaOH��Ӧ����C�Ľṹ��ʽΪ ____________________________��
(3)д��Aת��ΪC�Ļ�ѧ����ʽ��__________________________________________________________
(4)����C�к��еĹ����ŵĻ�ѧʵ�鷽����_____________________________________________________________________________________________________________________________________
(5)д��E�Ľṹ��ʽ��____________________��H�Ľṹ��ʽ��________________________________
(6)�����ϳɹ�����û���漰���ķ�Ӧ��������_________________����д��ţ�
A��ȡ����Ӧ�� b . �ӳɷ�Ӧ�� c. ��ȥ��Ӧ�� d. ������Ӧ�� e. ��ԭ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ȷ��ʾ���з�Ӧ�����ӷ���ʽ��
A. ��ʯī���缫���CuCl2��Һ��2Cl-+ 2H2O![]() 2OH-+Cl2��+H2��
2OH-+Cl2��+H2��
B. 0.01mol/L NH4A1(SO4)2��Һ��0.02 mol/L Ba(OH)2��Һ�������ϣ�Al3++2SO42-+2Ba2++4OH-=2BaSO4��+AlO2-+2H2O
C. CaCO3����CH3COOH ��CaCO3+2CH3COOH==Ca2++2CH3COO-+CO2��+H2O
D. Ca(HCO3)2��Һ�����NaOH ��Һ��Ӧ��Ca2++HCO3-+OH-=CaCO3��+H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ʵ��������������ó��Ľ�����ȷ����
ѡ�� | ʵ����������� | ���� |
A | �������м���Ũ���ᣬ����ú�ɫ����״���壬���ų��̼�����ζ���� | Ũ�����������ˮ�Ժ���ˮ�� |
B | ����ɫʯ����ֽ�ϵμ�������ˮ����ֽ��Ե�ʺ�ɫ���м�Ϊ��ɫ | ��ˮ�����������л�ԭ�� |
C | ±����Y��NaOH��Һ���Ⱥ�������ϡ���ᣬ�ٵμ�AgNO3��Һ��������ɫ���� | ±����Y�к�����ԭ�� |
D | ȡ5 mL 0.1 mol��L��1KI��Һ������1 mL 0.1 mol��L��1FeCl3��Һ����ȡ��Һ����ˮ�����KSCN��Һ����Һ���Ѫ��ɫ | Fe3����I���������ķ�ӦΪ���淴Ӧ |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и�����̬�⻯����ȶ�����ǿ������˳�����е���
A. HI HCl H2S PH3
B. PH3 H2S HCl HBr
C. HF HCl H2S SiH4
D. NH3 PH3 H2S HCl
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com