
| A. | 将pH=5的CH3COOH溶液稀释100倍 | |
| B. | 0.05mol/L H2SO4与0.10mol/L NaOH溶液以等体积混合 | |
| C. | pH=2的盐酸和pH=12的氨水两种溶液以等体积混合 | |
| D. | pH=1的H2SO4与0.10mol/L 的Ba(OH)2溶液以等体积混合 |
分析 A.pH=5的CH3COOH溶液稀释100倍,pH接近7,仍为酸性;
B.c(H+)=0.05mol/L×2=0.1mol/L,c(OH-)=0.1mol/L,等体积混合,n(H+)=n(OH-),为中性;
C.pH=2的盐酸中c(H+)=0.01mol/L,pH=12的氨水中c(NH3.H2O)>0.01mol/L;
D.pH=1的H2SO4中c(H+)=0.1mol/L,0.10mol/L 的Ba(OH)2溶液中c(OH-)=0.1mol/L×2=0.2mol/L.
解答 解:A.pH=5的CH3COOH溶液稀释100倍,pH接近7,仍为酸性,则c(H+)略小于1×10-7mol/L,故A不选;
B.c(H+)=0.05mol/L×2=0.1mol/L,c(OH-)=0.1mol/L,等体积混合,n(H+)=n(OH-),为中性,则c(H+)一定等于1×10-7mol/L,故B选;
C.pH=2的盐酸中c(H+)=0.01mol/L,pH=12的氨水中c(NH3.H2O)>0.01mol/L,等体积混合时碱过量,则溶液显碱性,c(H+)小于1×10-7mol/L,故C不选;
D.pH=1的H2SO4中c(H+)=0.1mol/L,0.10mol/L 的Ba(OH)2溶液中c(OH-)=0.1mol/L×2=0.2mol/L,则溶液显碱性,c(H+)小于1×10-7mol/L,故D不选;
故选B.
点评 本题考查酸碱混合的计算,为高频考点,把握pH与浓度的换算、酸碱混合的过量判断为解答的关键,侧重分析与计算能力的考查,注意常温时pH=7为中性,题目难度不大.


科目:高中化学 来源:2016-2017学年陕西西藏民族学院附中高二上月考二化学卷(解析版) 题型:填空题
研究化学反应中的能量变化有重要意义。请根据学过的知识回答下列问题:
Ⅰ.(1)已知一氧化碳与水蒸气反应过程的能量变化如图所示:
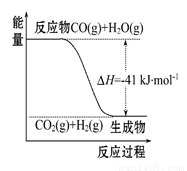
①反应的热化学方程式为 。
②已知:C(s)+H2O(g)=CO(g)+H2(g) ΔH=+131 kJ·mol-1,
则C(s)+CO2(g)=2CO(g) ΔH= 。
(2)化学反应可视为旧键断裂和新键形成的过程。化学键的键能是形成(或拆开)1 mol化学键时释放(或吸收)的能量。已知:N≡N键的键能是948.9 kJ·mol-1,H—H键的键能是436.0 kJ·mol-1;N—H键的键能是391
mol化学键时释放(或吸收)的能量。已知:N≡N键的键能是948.9 kJ·mol-1,H—H键的键能是436.0 kJ·mol-1;N—H键的键能是391 .55 kJ·mol-1。则N
.55 kJ·mol-1。则N 2(g)+3H2(g)=2NH3(g) ΔH= 。
2(g)+3H2(g)=2NH3(g) ΔH= 。
Ⅱ.下图是一个化学过程的示意图,回答下列问题:

(1)甲池是 装置,乙装置中电极A的名称 。
(2)甲装置中通入CH4的电极反应式为 ,乙装置中电极B(Ag)的电极反应式为 ,丙装置中D极的产物是 (写化学式)。
(3)一段时间,当丙池中产生112 mL(标准状况下)气体时,均匀搅拌丙池,所得溶液在25℃时的pH= 。(已知:NaCl溶液足量,电解后溶液体积为500 mL)。若要使丙池恢复电解前的状态,应向丙池中通入 (写化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用丁达尔效应可区分胶体和溶液 | |
| B. | 煤可经分馏获得洁净的燃料 | |
| C. | 非金属材料中不可以含有金属元素 | |
| D. | 电解氯化镁饱和溶液,可制得金属镁 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.2mol | B. | 0.4mol | C. | 0.6mol | D. | 0.8mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷的燃烧热△H=-890.3kJ/mol,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3 kJ/mol | |
| B. | 一定条件下,将0.5 mol N2和1.5 molH2置于密闭容器中充分反应生成NH3放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)?2NH3(g)△H=-38.6 kJ/mol | |
| C. | 在101kPa时,2gH2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)═2H2O(l)△H=-571.6 kJ/mol | |
| D. | HCl和NaOH反应的中和热△H=-57.3 kJ/mol,则H2SO4和Ba(OH)2反应的反应热△H=2×(-57.3)kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验步骤 | 实验现象 | 结论 |
| ①在蒸馏水中加少量明矾,搅拌静置 | 明矾全部溶解 | |
| ②在浑浊的天然水中加少量明矾,搅拌静置 | 有絮状沉淀生成,天然水变澄清 | |
| ③在浑浊的天然水中加少量硫酸,搅拌静置 | ||
| ④在浑浊的天然水中加少量硫酸钾,搅拌静置 | ||
| ⑤在浑浊的天然水中加氯化铝,搅拌静置 | 有絮状沉淀生成,天然水变 澄清 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用BaCl2溶液鉴别Na2CO3和Na2SO4溶液 | |
| B. | 用淀粉溶液检验食盐中是否添加KIO3 | |
| C. | 用焰色反应并透过蓝色钴玻璃检验NaCl中是否混有KCl | |
| D. | 用溴水鉴别乙烯和二氧化硫两种气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 32:18 | B. | 16:11 | C. | 8:11 | D. | 16:9 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
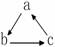 (“→”表示一步完成)关系相互转化的是( )
(“→”表示一步完成)关系相互转化的是( )| 选项 | A | B | C | D |
| a | HNO2 | CH2=CH2 | NaOH | Fe |
| b | NO | CH3CH2Br | NaHCO3 | FeCl3 |
| c | NO2 | CH3CH2OH | Na2CO3 | FeCl2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com