
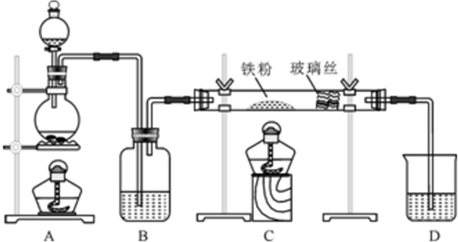
分析 由制备氯化铁的实验装置可知,A中浓盐酸与二氧化锰反应生成氯气,B中浓硫酸干燥氯气,C中Fe与氯气反应生成氯化铁,D中NaOH溶液吸收尾气;
若制备无水氯化亚铁,A中浓硫酸与NaCl反应生成HCl,B中浓硫酸干燥HCl,C中炽热铁屑中与HCl反应生成无水氯化亚铁,D为尾气处理,但导管在液面下可发生倒吸,检验FeCl3常用的试剂为KSCN溶液,溶液为血红色,以此来解答.
解答 解:(1)由制备氯化铁的实验装置可知,A中浓盐酸与二氧化锰反应生成氯气,反应为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,装置B中加入的试剂是浓硫酸,
故答案为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;浓硫酸;
(2)制取无水氯化亚铁的实验中,装置A用来制取HCl,Fe与HCl反应生成氢气,可知尾气的成分是HCl和H2.若仍用D的装置进行尾气处理,存在的问题是发生倒吸、可燃性气体H2不能被吸收,
故答案为:HCl;HCl和H2;发生倒吸、可燃性气体H2不能被吸收;
(3)若操作不当,制得的FeCl2 会含有少量FeCl3,检验FeCl3常用的试剂是KSCN溶液,可观察到溶液为血红色可检验,故答案为:KSCN溶液.
点评 本题考查物质的制备实验,为高频考点,把握氯气、HCl的制备原理及Fe的化学性质为解答的关键,侧重分析与实验能力的考查,注意元素化合物与实验的结合,题目难度不大.


 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案科目:高中化学 来源: 题型:解答题

 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “测定气体摩尔体积”实验中,若温度高于0℃,气体摩尔体积一定大于22.4L/mol | |
| B. | “浓硫酸稀释”实验中,将水慢慢注入浓硫酸中,并不断搅拌 | |
| C. | “实验室制取氢气”实验中,收集装置与氯化氢气体的收集装置相同 | |
| D. | “萃取”实验中,振荡后,需要打开分液漏斗活塞,使漏斗内气体放出 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | PX 项目的主要产品对二甲苯属于饱和烃 | |
| B. | 食用花生油和鸡蛋清都能发生水解反应 | |
| C. | 包装用材料聚乙烯和聚氯乙烯都属于烃 | |
| D. | 保护加酶洗衣粉的洗涤效果,应用沸水溶解洗衣粉 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 定量分析--测沸点 | |
| B. | 定性分析--滴入酸性高锰酸钾溶液 | |
| C. | 定量分析--使用银氨溶液 | |
| D. | 定性分析--与新制氢氧化铜悬浊液共热 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
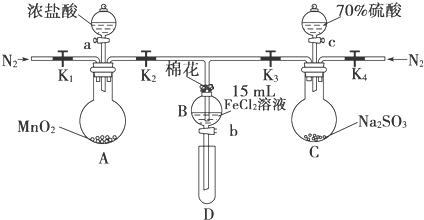
| 过程Ⅳ,B溶液中含有的离子 | 过程Ⅵ,B溶液中含有的离子 | |
| 甲 | 有Fe3+无Fe2+ | 有SO42- |
| 乙 | 既有Fe3+又有Fe2+ | 有SO42- |
| 丙 | 有Fe3+无Fe2+ | 有Fe2+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com