
| A、中性溶液的pD等于7 |
| B、在D2O中溶解0.01mol DCl配成1L溶液,则pD等于2.0 |
| C、在D2O中溶解0.01mol NaOD配成1L溶液,则pD等于12.0 |
| D、达当由重水电离出来的c(D+)等于10-13mol/L时,溶液的pD等于1或13 |
| 1.6×10-15 |
| 10-13 |
| 1.6×10-15 |
| 0.01 |
| 1.6×10-15 |
| 10-13 |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
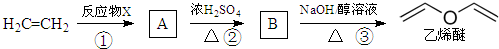
| A、X可能为Br2 |
| B、X可能为HO-Cl |
| C、乙烯醚易溶于水 |
| D、①②③反应类型依次为加成、取代和消去 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na与足量O2反应,随温度升高生成Na2O的速率逐渐加快 |
| B、Na2O和Na2O2中的阴阳离子个数比不相等 |
| C、用洁净铂丝蘸取溶液进行焰色反应,火焰呈黄色说明原溶液中有Na+无K+ |
| D、25℃,NaHCO3在水中的溶解度比Na2CO3的小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碳酸钙与盐酸的反应:CaCO3+2H+=Ca2++CO2↑+H2O |
| B、等物质的量的MgCl2、Ba(OH)2和HCl溶液混合:Mg2++2OH-=Mg(OH)2↓ |
| C、氧化铜与稀H2SO4反应:CuO+2H+=Cu2++H2O |
| D、金属钠跟水反应:2Na+2H2O=2Na++2OH-+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、反应体系中所有含氧物质中均有18O |
| B、反应体系中含18O的分子有2种 |
| C、可能生成45g乙酸乙酯 |
| D、不可能生成88g乙酸乙酯 |
查看答案和解析>>
科目:高中化学 来源: 题型:
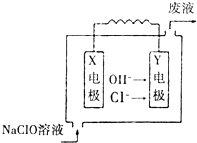 电解池、原电池对于金属冶炼、实验室研究具有十分重要的意义.
电解池、原电池对于金属冶炼、实验室研究具有十分重要的意义.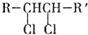 (R、R表示烃基)则该原电池的负极反应式为
(R、R表示烃基)则该原电池的负极反应式为查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 实验操作及现象 | 实验目的或结论 |
| A | 测同浓度的Na2CO3、CH3COONa 溶液的PH值前者大 | 酸性强弱:CH3COOH 比H2CO3强 |
| B | 向某溶液加入盐酸酸化的氯化钡溶液有沉淀产生 | 说明此溶液中一定含SO42- |
| C | 向Na2SiO3溶液中通入CO2 出现浑浊 | 非金属性强弱:C>Si |
| D | 比较H2O和H2S的沸点前者大 | 非金属性:O>S |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、轮船水线下的船体上装一定数量的锌块 |
| B、镀锌铁比镀锡铁耐用 |
| C、纯锌与稀硫酸反应时,滴入少量CuSO4溶液后速率增大 |
| D、铝片不用特殊方法保护 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③⑤⑦⑧ | B、②④ |
| C、②④⑧ | D、②④⑦ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com