
【题目】单质A、B、C和甲、乙、丙、丁、戊五种化合物有下图所示转换关系,工业上电解熔融的甲可制取金属A。请回答:
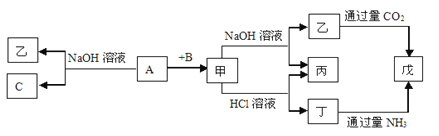
(1)写出下列物质的化学式:A__________、甲__________。
(2)写出乙物质的溶液中通入过量CO2的现象:________________________________;
(3)写出丁与过量氨水反应的离子方程式:__________________________________。
(4)写出A与NaOH溶液反应的化学方程式:__________________________________。
【答案】Al Al2O3 产生白色胶状沉淀 Al3++3NH3·H2O===Al(OH)3↓+3NH4+ 2Al+2NaOH+2H2O==2NaAlO2+3H2↑
【解析】
试题由图中信息可知,单质A可以与氢氧化钠溶液反应生成单质C,A和B反应生成的甲,甲既能和盐酸反应又能和氢氧化钠溶液反应,且可用于工业上电解法制取金属A,综合题中其他转化,可以判断出A为铝、B为氧气、C为氢气、甲为氧化铝、乙为偏铝酸钠、丙为水、丁为氯化铝、戊为氢氧化铝。
(1)A 的化学式为Al、甲的化学式为Al2O3 。
(2)偏铝酸钠溶液中通入过量CO2的现象是产生白色胶状沉淀;
(3)氯化铝与过量氨水反应的离子方程式为Al3++3NH3·H2O===Al(OH)3↓+3NH4+ 。
(4)Al与NaOH溶液反应的化学方程式为2Al+2NaOH+2H2O==2NaAlO2+3H2↑ 。


科目:高中化学 来源: 题型:
【题目】在密闭真空容器中加入一定量纯净的氨基甲酸铵固体(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s) ![]() 2NH3(g)+CO2(g) ΔH>0。下列说法中正确的是( )
2NH3(g)+CO2(g) ΔH>0。下列说法中正确的是( )
A.密闭容器中气体的平均相对分子质量不变,则该反应达到平衡状态
B.密闭容器中气体的密度不变,则该反应达到平衡状态
C.再加入一定量氨基甲酸铵,可加快正反应速率
D.保持温度不变,压缩体积,可使正、逆反应速率都增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列与金属腐蚀有关的说法正确的是( )
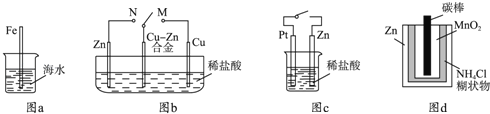
A.图a中,插入海水中的铁棒,越靠近底端腐蚀越严重
B.图b中,开关由M改置于N时,Cu﹣Zn合金的腐蚀速率减小
C.图c中,接通开关时Zn腐蚀速率增大,Zn上放出气体的速率也增大
D.图d中,Zn﹣MnO2干电池自放电腐蚀主要是由MnO2的氧化作用引起的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将0.65g的锌加到50mL 1mol/L 盐酸中发生如下反应:Zn+2HCl=ZnCl2+H2↑,生成0.224L的H2(标准状况下),则:
(1)填空:0.65g的锌的物质的量___________,生成的0.224L的氢气的物质的量___________,反应前盐酸的物质的量___________,实际参加反应的盐酸的物质的量___________,
(2)计算:若反应完成后体积不变,溶液中剩余盐酸的物质的量浓度_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以高硫铝土矿(主要成分为Al2O3、Fe2O3、SiO2,少量FeS2和金属硫酸盐)为原料,生产氧化铝并获得Fe3O4的部分工艺流程如下:
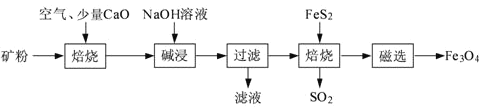
(1)粉碎高硫铝土矿石的目的是______。
(2)焙烧时发生氧化还原反应:______FeS2+______O2![]() ______Fe2O3+______SO2↑,配平该方程式。
______Fe2O3+______SO2↑,配平该方程式。
(3)碱浸时发生反应的化学方程式为______。
(4)过滤后向滤液中通入过量的CO2气体,反应的离子方程式为______。
(5)“过滤”得到的滤渣中含有大量的Fe2O3。Fe2O3与FeS2混合后在缺氧条件下焙烧生成Fe3O4和SO2,理论上完全反应消耗的n(FeS2):n(Fe2O3)=______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在杠杆的两端分别挂着质量相同的铝球和铁球,此时杠杆平衡。然后将两球分别浸没在溶液质量相等的稀烧碱溶液和硫酸铜溶液中一段时间,如图所示。下列说法正确的是( )
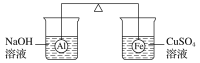
A.铝球表面有气泡产生,且有白色沉淀生成,杠杆不平衡
B.铝球表面有气泡产生,溶液澄清;铁球表面有红色物质析出,杠杆右边下沉
C.反应后去掉两烧杯,杠杆仍平衡
D.右边球上出现红色,左边溶液的c(OH-)增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】假设烷烃的通式为![]() ,以下物理量随n的增加而减小的是 ( )
,以下物理量随n的增加而减小的是 ( )
A. 1mol烷烃中共价键的数目B. 1mol烷烃完全燃烧时的耗氧量
C. 一氯代物的种类D. 氢元素的含量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】结构决定性质,有机化合物的结构也是研究有机物性质的基础。
(1)烷基是烷烃失去一个或若干氢原子后剩下的电中性的原子团,请在方框内写出甲基的电子式_______。

(2)有一类有机物,它的一卤代物只有一种,如![]() 、
、![]() 等。请写出另外两种满足该条件烷烃的结构简式,并用系统命名法命名。
等。请写出另外两种满足该条件烷烃的结构简式,并用系统命名法命名。
结构简式 | _______ | _______ |
系统命名 | _______ | _______ |
(3)烷烃都是由共价键形成的有机物,若用I表示一个烷烃分子中的共价键数,n表示该烷烃的碳原子数,则丙烷(![]() )的共价键数
)的共价键数![]() ____________﹔若某烷烃的共价键数
____________﹔若某烷烃的共价键数![]() ,则
,则![]() ____________。
____________。
(4)烃的结构主要由碳原子的连接顺序决定,因此我们常通过键线式来表示烃的结构,其中每个端点和拐角都代表一个碳,每个碳原子连接的氢原子都不表示出来。A、B、C分别表示三种物质的空间立体结构:
A. 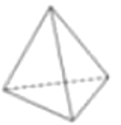 B.
B.  C.
C. 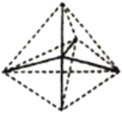
①上述结构中的C不可能是烃,理由是______________________________。
②B分子的分子式是__________________,其一氯代物共有____________种。
③在结构A的每两个碳原子之间插入一个![]() 原子团,可以形成金刚烷的结构,写出金刚烷的分子式__________________。
原子团,可以形成金刚烷的结构,写出金刚烷的分子式__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关叙述正确的是
①水的摩尔质量是18g
②0.5molH2的体积为11.2L
③1 mol 水中含有 2 mol 氢和 1mol 氧
④1mol 任何物质都约含有6.02×1023个分子
⑤0.5mol H2SO4含有的原子数目为3.5NA
⑥只有在标准状况下,体积相同的任何气体所含的分子数相同
⑦质量分数为40%的硫酸溶液与等体积的水混合,所得溶液浓度大于20%
⑧物质的量浓度为4mol/L 的硫酸溶液与等质量的水混合,所得溶液浓度小于2mol/L
A. ①③④⑤⑦⑧ B. ②⑤⑦⑧ C. ⑤⑦⑧ D. ⑤⑦
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com