
| 消耗量 |
| 起始量 |
| x |
| 3+x |
| 消耗量 |
| 起始量 |
| 0.75mol |
| 3mol |
| 0.75×0.75 |
| 2.25 |
| y2 |
| (5-y) |
| 1mol |
| 5mol+1mol |


 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案科目:高中化学 来源: 题型:
| A、有盐类物质生成 |
| B、有酯类物质生成 |
| C、有醇类物质生成 |
| D、有酸类物质生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
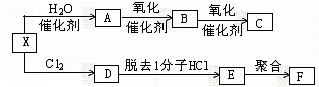
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、往饱和碳酸钠溶液中通入足量CO2 ,溶液变浑浊 |
| B、往同物质的量浓度的两种溶液中滴入等量酚酞,Na2CO3 溶液红色更深 |
| C、将澄清石灰水加入NaHCO3 溶液中不产生沉淀,加入Na2CO3 溶液中产生白色沉淀 |
| D、同物质的量浓度同体积的两种溶液与Ca(OH)2 反应均完全转变为CaCO3,Na2CO3溶液消耗的大于NaHCO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 3 |
| A、混合物中含有0.5molFeS |
| B、混合物中含有0.1mol FeO |
| C、参加反应的HNO3为1mol |
| D、氧化产物Fe3+为0.15mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
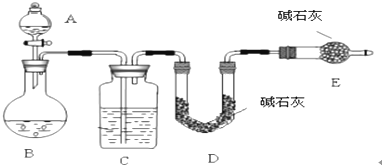
查看答案和解析>>
科目:高中化学 来源: 题型:
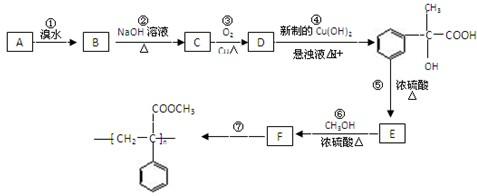
查看答案和解析>>
科目:高中化学 来源: 题型:
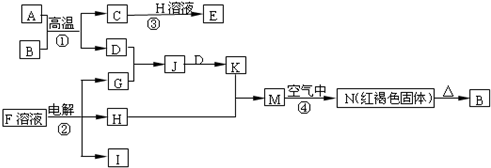
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com