
【题目】下列说法不正确的是
A.“光化学烟雾”、“硝酸型酸雨”的形成都与氮氧化合物有关
B.![]() 可作阻燃剂,因此可以用于灭火
可作阻燃剂,因此可以用于灭火
C.![]() 可用于制造光导纤维,其性质稳定,不溶于强酸、强碱
可用于制造光导纤维,其性质稳定,不溶于强酸、强碱
D.焰火的五彩缤纷是某些金属元素的性质的展现
 考前必练系列答案
考前必练系列答案科目:高中化学 来源: 题型:
【题目】铁镁合金是目前已发现的储氢密度较高的储氢材料之一,其晶胞结构如图所示(黑球代表 Fe,白球代表 Mg)。则下列说法不正确的是
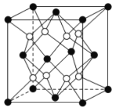
A.铁镁合金的化学式为 Mg2FeB.晶体中存在的化学键类型为金属键、离子键
C.晶胞中 Fe与 Mg的配位数均为4D.该晶胞的质量是![]() g
g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】邻乙酰氨基酚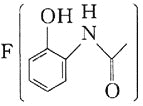 是合成抗肿瘤药物嘧啶苯芥的中间体,其合成路线如下所示
是合成抗肿瘤药物嘧啶苯芥的中间体,其合成路线如下所示![]() 部分反应条件、试剂及生成物略去
部分反应条件、试剂及生成物略去![]() 。
。
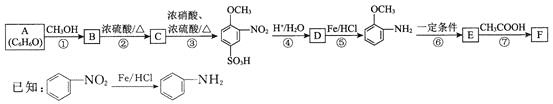
请回答下列问题:
![]() 中所含官能团的电子式为________________,B的化学名称为________________,F的分子式为________________。
中所含官能团的电子式为________________,B的化学名称为________________,F的分子式为________________。
![]() 反应
反应![]() 和反应
和反应![]() 的反应类型分别为________、________。
的反应类型分别为________、________。
![]() 反应
反应![]() 的化学方程式为________________________________。
的化学方程式为________________________________。
![]() 由B经反应
由B经反应![]() 制取D的目的是________________________________。
制取D的目的是________________________________。
![]() 同时满足下列条件的F的同分异构体有________种
同时满足下列条件的F的同分异构体有________种![]() 不考虑立体异构
不考虑立体异构![]() 。
。
![]() 属于芳香化合物且含有氨基
属于芳香化合物且含有氨基
![]() 能与
能与![]() 溶液反应放出
溶液反应放出![]()
其中核磁共振氢谱中有5组峰的结构简式为________________![]() 任写一种即可
任写一种即可![]() 。
。
![]() 参照上述流程,以甲苯为原料
参照上述流程,以甲苯为原料![]() 无机试剂任选
无机试剂任选![]() 设计制备邻甲基苯胺的合成路线:_______________________________________________________________________________。
设计制备邻甲基苯胺的合成路线:_______________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Y具有抗菌、消炎作用,可由化合物X制得。

下列关于化合物X、Y说法正确的是( )
A.X分子中含有三种官能团
B.X、Y均能与FeCl3溶液发生显色反应
C.X、Y分子均能发生氧化、还原、取代反应
D.1 mol X、Y分别与足量NaOH反应,消耗NaOH的最多量相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】孔雀石的主要成分是![]()
(1)试写出孔雀石高温分解的化学方程式:________________________________________________。
(2)试以(1)中所得金属氧化物为原料,分别采用湿法冶炼和高温冶炼的方式制取金属铜。供选择的试剂有①木炭、②铁屑、③生石灰、④稀硫酸,不得另选其他试剂,写出下列主要反应的化学方程式。
A.湿法冶炼: ____________________________;
B.高温冶炼: _______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.黄铁矿,主要成分是FeS,它只是生产硫酸的工业原料
B.利用铁的活泼性可以从铜盐中置换出铜单质,是青铜器时代湿法炼铜的原理
C.从海水中提取镁时需要先往海水中加入石灰乳
D.玻璃、玛瑙、石英、陶瓷、水泥都是传统的硅酸盐工业产品
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,通过下列反应可实现燃煤烟气中的硫的回收:SO2(g)+2CO(g)![]() 2CO2(g)+S(l) ΔH<0。一定温度下,在容积为2L的恒容密闭容器中,1molSO2和nmolCO发生反应,2min后达到平衡,生成2amolCO2。下列说法中正确的是( )
2CO2(g)+S(l) ΔH<0。一定温度下,在容积为2L的恒容密闭容器中,1molSO2和nmolCO发生反应,2min后达到平衡,生成2amolCO2。下列说法中正确的是( )
A.反应前2min的平均速率υ(SO2)=0.1amol/(L·min)
B.当混合气体的物质的量不再改变时,反应达到平衡状态
C.平衡后保持其他条件不变,从容器中分离出部分硫,平衡向正反应方向移动
D.平衡后保持其他条件不变,升高温度和加入催化剂,SO2的转化率均增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应的快慢和限度对人类生产生活有重要的影响。800℃时,A、B、C三种气体在恒容密闭容器中反应时的浓度变化如图所示,回答下列问题:

(1)该反应的生成物是________。
(2)2min内,C的反应速率为________。
(3)该反应的化学方程式为________。
(4)在其他条件下,测得A的反应速率为![]() ,此时的反应速率与800℃时相比_____。
,此时的反应速率与800℃时相比_____。
A.比800℃时慢 B.比800℃时快 C.和800℃时速率一样
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化还原是一类重要的反应。
(1)已知反应2I-+2Fe3+=I2+2Fe2+,反应中还原剂是_________,氧化性Fe3+______I2 (填“ < ”或“ > ”) 。
(2)在2Na2O2+2CO2=2Na2CO3+O2反应中,若转移3mol电子,则所产生的氧气在标准状况下的体积为___________L。
(3)在xR2++yH++O2═mR3++nH2O的离子方程式中,对系数m和R2+、R3+判断正确的是__。
A.m=y,R3+是还原剂 B.m=2y,R2+被氧化
C.m=2,R3+是氧化剂 D.m=4,R2+是还原剂
(4)用双线桥标出反应2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O中电子转移的方向和数目_________。
(5)氯气和石英砂、碳粉共热可发生反应:SiO2+2C+2Cl2![]() SiCl4+2CO当反应消耗6g碳时,生成还原产物_________mol。
SiCl4+2CO当反应消耗6g碳时,生成还原产物_________mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com