
·ÖĪö £Ø1£©Ģ¼ĖįĒāøłĄė×ÓµÄĖ®½ā³Ģ¶Č“óÓŚĘäµēĄė³Ģ¶Č£¬ČÜŅŗ³Ź¼īŠŌ£¬Ōņc£ØOH-£©£¾c£ØH+£©”¢c£ØNa+£©£¾c£ØHCO3-£©£¬¾Ż“ĖÅŠ¶ĻĢ¼ĖįĒāÄĘČÜŅŗÖŠµÄĄė×ÓÅØ¶Č“óŠ”£»
£Ø2£©øł¾ŻĢ¼ĖįĒāÄĘČÜŅŗÖŠµÄµēŗÉŹŲŗć·ÖĪö£»
£Ø3£©øł¾ŻĢ¼ĖįĒāÄĘČÜŅŗÖŠµÄĪļĮĻŹŲŗć½ā“š£®
½ā“š ½ā£ŗ£Ø1£©Ģ¼ĖįĒāÄĘČÜŅŗÖŠ£¬Ģ¼ĖįĒāøłĄė×ÓµÄĖ®½ā³Ģ¶Č“óÓŚĘäµēĄė³Ģ¶Č£¬ČÜŅŗ³Ź¼īŠŌ£¬Ōņc£ØOH-£©£¾c£ØH+£©”¢c£ØNa+£©£¾c£ØHCO3-£©£¬ČÜŅŗÖŠĄė×ÓÅØ¶Č“óŠ”ĪŖ£ŗc£ØNa+£©£¾c£ØHCO3-£©£¾c£ØOH-£©£¾c£ØH+£©£¾c£ØCO32-£©£¬
¹Ź“š°øĪŖ£ŗc£ØNa+£©£¾c£ØHCO3-£©£¾c£ØOH-£©£¾c£ØH+£©£¾c£ØCO32-£©£»
£Ø2£©øł¾ŻĢ¼ĖįĒāÄĘČÜŅŗÖŠµÄµēŗÉŹŲŗćæÉµĆ£ŗc£ØNa+£©+c£ØH+£©=c£ØHCO3-£©+c£ØOH-£©+2c£ØCO32-£©£¬
¹Ź“š°øĪŖ£ŗc£ØHCO3-£©+c£ØOH-£©+2c£ØCO32-£©£»
£Ø3£©øł¾ŻĢ¼ĖįĒāÄĘČÜŅŗµÄĪļĮĻŹŲŗćæÉµĆ£ŗc£ØNa+£©=c£ØHCO3-£©+c£ØCO32-£©+c£ØH2CO3£©£¬
¹Ź“š°øĪŖ£ŗc£ØHCO3-£©+c£ØCO32-£©+c£ØH2CO3£©£®
µćĘĄ ±¾Ģāæ¼²éĮĖĄė×ÓÅØ¶Č“óŠ”±Č½Ļ£¬ĢāÄæÄѶČÖŠµČ£¬Ć÷Č·ŃĪµÄĖ®½āŌĄķĪŖ½ā“š¹Ų¼ü£¬×¢ŅāÕĘĪÕµēŗÉŹŲŗć”¢ĪļĮĻŹŲŗćµÄŗ¬Ņå¼°Ó¦ÓĆ·½·Ø£¬ŹŌĢāÅąŃųĮĖѧɜµÄ·ÖĪö”¢Ąķ½āÄÜĮ¦¼°Įé»īÓ¦ÓĆÄÜĮ¦£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ijĪĀ¶ČŹ±£¬KW=10-12£¬“ĖĪĀ¶ČĻĀPH=6µÄČÜŅŗŅ»¶ØĻŌĖįŠŌ | |
| B£® | 25”ꏱ£¬0.1mol/LµÄNaHSO3ČÜŅŗpH=4£¬ĖµĆ÷HSO3-ŌŚĖ®ČÜŅŗÖŠÖ»“ęŌŚµēĄė | |
| C£® | NH4Cl”¢CH3COONa”¢NaHCO3”¢NaHSO4ČÜÓŚĖ®£¬¶ŌĖ®µÄµēĄė¶¼ÓŠ“Ł½ų×÷ÓĆ | |
| D£® | Ļ”ŹĶ 0.1mol/L CH3COONaČÜŅŗ¹ż³ĢÖŠ£¬c£ØOH-£©/c£ØCH3COO-£©Ōö“ó |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | AlCl3 | B£® | KCl | C£® | CaCl2 | D£® | LiCl |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ³£ĪĀĻĀ¼×ÄÜÓėĒāĘųÖ±½Ó»ÆŗĻ£¬ŅŅ²»ÄÜ | |
| B£® | ¼×µÄŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļĖįŠŌ±ČŅŅĒæ | |
| C£® | ¼×µĆµ½µē×ÓÄÜĮ¦±ČŅŅĒæ | |
| D£® | ¼×”¢ŅŅŠĪ³ÉµÄ»ÆŗĻĪļÖŠ£¬¼×ĻŌøŗ¼Ū£¬ŅŅĻŌÕż¼Ū |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
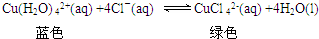
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÓĆĶŠÅĢĢģĘ½³ĘČ”28.6g Na2CO3•10H2O¾§Ģå | |
| B£® | ½«Na2CO3¹ĢĢå·ÅČėČŻĘ÷ĘæÖŠ£¬¼ÓĖ®ÖĮæĢ¶ČĻß | |
| C£® | ¶ØČŻŹ±ø©ŹÓŅŗĆę£¬ĖłµĆČÜŅŗÅضČĘ«µĶ | |
| D£® | ¼ÓĖ®Ź±²»É÷³¬¹żæĢ¶ČĻߣ¬ÓĆ½ŗĶ·µĪ¹ÜÖ±½ÓĪü³ö¶ąÓąŅŗĢå |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ČÜŅŗ | B£® | ½ŗĢå | ||
| C£® | Šü×ĒŅŗ | D£® | »„²»ĻąČŻµÄĮ½ÖÖŅŗĢå |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
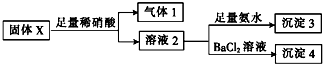
| A£® | ĘųĢå1Ņ»¶Øŗ¬NOæÉÄÜŗ¬CO2 | |
| B£® | ³Įµķ3Ņ»¶Øŗ¬Mg£ØOH£©2Ņ»¶Ø²»ŗ¬Al£ØOH£©3 | |
| C£® | ³Įµķ4æÉÄÜĪŖBaCO3”¢BaSO3»ņ¶žÕß»ģŗĻĪļ | |
| D£® | ¹ĢĢå·ŪÄ©XÖŠŅ»¶ØÓŠMgCl2ŗĶNa2SO3£¬æÉÄÜÓŠKAlO2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ”¢¢ņ
”¢¢ņ £®
£®

²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com