
| A、1mol氢的质量是1g |
| B、1molCO的质量为28g?mol-1 |
| C、阿伏加德罗常数等于6.02×1023 |
| D、3.01×1023个SO2分子约是0.5mol |
| N |
| NA |
| N |
| NA |
| 3.01×1023 |
| 6.02×1023 |


 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案科目:高中化学 来源: 题型:
| A、12和6 | B、14和7 |
| C、16和8 | D、18和9 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、⑦⑨② | B、⑧③①② |
| C、⑥②①④ | D、⑤②⑩④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2Al+2NaOH+2H2O═2NaAlO2+3H2↑ 置换反应 |
| B、FeCl3溶于水发生的反应 复分解反应 |
| C、C2H5OH+HB→C2H5Br+H2O 复分解反应 |
| D、IBr+H2?HBr+HIO 氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
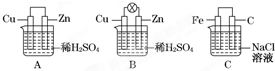 观察图A、B、C,回答下列问题:
观察图A、B、C,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
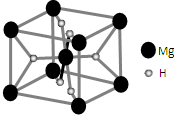 开发新型储氢材料是氢能利用的重要研究方向.
开发新型储氢材料是氢能利用的重要研究方向.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com