
 工业上,在强碱性条件下用电解法除去废水中的CN-,装置如图所示,依次发生的反应有:
工业上,在强碱性条件下用电解法除去废水中的CN-,装置如图所示,依次发生的反应有:| A、铁电极上发生的反应为Fe-2e-═Fe2+ |
| B、通电过程中溶液pH值不断增大 |
| C、为了使电解池连续工作,需要不断补充NaCl |
| D、除去1mol CN-,外电路至少需转移5mol电子 |


科目:高中化学 来源: 题型:
| A、乙烯能使酸性KMnO4溶液和溴水褪色,二者反应原理不相同 |
| B、交警用酸性重铬酸钾溶液检查司机是否饮酒过量时乙醇发生取代反应 |
| C、乙酸的分子式为CH3COOH,属于弱电解质 |
| D、苯分子中没有碳碳双键,因此苯不能发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 原子的最外层电子数相差1.请回答下列问题:
原子的最外层电子数相差1.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:

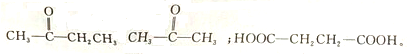
查看答案和解析>>
科目:高中化学 来源: 题型:
 C70是椭球状的多面体,如图所示.该结构的建立基于以下考虑:①C70分子中每个碳原子只跟相邻的3个碳原子形成化学键;②C70分子中只含有五边形和六边形;③多面体的顶点数、面数和棱边数的关系遵循欧拉定理:顶点数+面数-棱边数=2
C70是椭球状的多面体,如图所示.该结构的建立基于以下考虑:①C70分子中每个碳原子只跟相邻的3个碳原子形成化学键;②C70分子中只含有五边形和六边形;③多面体的顶点数、面数和棱边数的关系遵循欧拉定理:顶点数+面数-棱边数=2查看答案和解析>>
科目:高中化学 来源: 题型:
| A、有些金属晶体比原子晶体熔沸点高 |
| B、晶体只要有阴离子就一定有阳离子 |
| C、原子晶体中一定有非极性共价键 |
| D、分子晶体中不一定有共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、造价太高同时形成白色垃圾而引起环境污染 |
| B、太软,饮用和运输时很不方便 |
| C、相对玻璃透气性强,啤酒易被氧化而变质 |
| D、属有机物,能与啤酒互溶而不与雪碧、可口可乐等饮品互溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、一定条件下,密闭容器中充入1 mol N2和3 mol H2可生成2 mol NH3 |
| B、一定条件下,合成氨反应达到平衡状态.此后的10分钟内,以氮气浓度变化表示的平均反应速率数值为零 |
| C、增大体系压强,任何化学反应速率均增大 |
| D、化学平衡是一种动态平衡,条件改变,原平衡状态一般不会被破坏 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com