
【题目】氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的热点。
(1) NaBH4是一神重要的储氢载体,能与水反应生成NaBO2,且反应前后B的化合价不变,该反应的化学方程式为_________,反应消耗1molNaBH4时转移的电子数目为___________。
(2) H2S热分解可制氢气。反应方程式:2H2S(g)=2H2(g)+S2(g) △H;在恒容密闭容器中,测得H2S分解的转化率(H2S起始浓度均为c mol/L)如图1所示。图l中曲线a表示H2S的平衡转化率与温度的关系,曲线b表示不同温度下反应经过相同时间且未达到化学平衡时H2S的转化率。

①△H ______0(填“>”“<”或“=”);
②若985℃时,反应经t min达到平衡,此时H2S的转化率为40%,则t min内反应速率v(H2)=_____(用含c、t的代数式表示);
③请说明随温度升高,曲线b向曲线a接近的原因____________。
(3) 使用石油裂解的副产物CH4可制取H2,某温度下,向体积为2L的密闭容器中充入0.40mol CH4(g)和0.60molH2O(g)的浓度随时间的变化如下表所示:

①写出此反应的化学方程式_________,此温度下该反应的平衡常数是_________。
②3 min时改变的反应条件是_________(只填一种条件的改变)。
③一定条件下CH4的平衡转化率与温度、压强的关系如图2所示。则P1_________P2填“>”、“<”或“=“)。
【答案】 NaBH4+2H2O=NaBO2+4H2↑ 4NA或2.408×1024 > 0.4c/tmol/(L·min) 温度升高,反应速率加快,达到平衡的时间缩短 CH4+H2O![]() 3H2+CO 0.135 升高温度、增加水蒸气或减少CO <
3H2+CO 0.135 升高温度、增加水蒸气或减少CO <
【解析】(1)本题考查离子反应方程式的书写,BH4-中H显-1价,H2O中H显+1价,发生NaBH4+2H2O=NaBO2+4H2↑,1molNaBH4参加反应转移电子1×4mol=4mol,即电子数为4NA;(2)本题考查化学反应速率的计算、影响化学平衡移动的因素等,①根据图1,随着温度的升高,H2S的转化率增大,即正反应方向是吸热反应,△H>0;②H2S的转化率为40%,则生成氢气浓度为c×40%mol·L-1=0.4cmol·L-1,根据化学反应速率的数学表达式,v(H2)=0.4c/tmol/(L·min);③温度升高,反应速率加快,达到平衡的时间缩短;(3)考查化学平衡的计算,①根据信息,达到平衡时,v(CH4)=(0.2-0.1)/2mol/(L·min)=0.05 mol/(L·min),v(H2)=0.3/2mol/(L·min)=0.15mol/(L·min),两者的系数之比为0.05:0.15=1:3,另一种气体为CO,因此反应方程式为CH4+H2O ![]() 3H2+CO;
3H2+CO;
CH4+H2O ![]() 3H2+CO
3H2+CO
起始(mol·L-1) 0.2 0.3 0 0
变化: 0.1 0.1 0.3 0.1
平衡: 0.1 0.2 0.3 0.1 化学平衡常数的表达式K=c3(H2)×c(CO)/[c(CH4)×c(H2O)]=0.33×0.1/(0.1×0.2)=0.135;②CH4的浓度减小,H2浓度增大,说明反应向正反应方向移动,改变的条件是升高温度、增加水蒸气或减少CO;③作等温线,压强增大,平衡向逆反应方向移动,CH4的转化率降低,即P1<P2。


 走进文言文系列答案
走进文言文系列答案科目:高中化学 来源: 题型:
【题目】下列各组物质分类正确的是( )
电解质 | 非电解质 | 化合物 | |
A | H2SO4 | Cl2 | NaCl |
B | NaOH | 酒精 | N2 |
C | CuSO4 | 水银 | CO2 |
D | BaSO4 | 蔗糖 | KClO3 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在化学分析中,常需用KMnO4标准溶液,由于KMnO4晶体在室温下不太稳定,因而很难直接配制准确物质的量浓度的KMnO4溶液。实验室一般先称取一定质量的KMnO4晶体,粗配成大致浓度的KMnO4溶液,再用性质稳定、相对分子质量较大的基准物质草酸钠[ Na2C2O4 相对分子质量=134.0 ]对粗配的KMnO4溶液进行标定,测出所配制的KMnO4溶液的准确浓度,反应原理为: 5C2O42-+2MnO4-+16H+===10CO2↑+2Mn2++8H2O以下是标定KMnO4溶液的实验步骤:
步骤一:先粗配浓度约为0.15mol/L的KMnO4溶液500mL。
步骤二:准确称取Na2C2O4固体mg放入锥形瓶中,用蒸馏水溶解并加稀硫酸酸化,加热至70~80℃,用步骤一所配KMnO4溶液进行滴定。记录相关数据。
步骤三: 。
步骤四:计算得KMnO4溶液的物质的量浓度。
试回答下列问题:
(1)下左图为整个过程中可能使用的仪器的部分结构(有的仪器被放大),
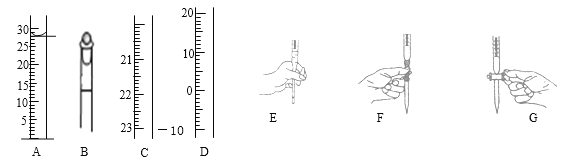
A图中液面所示溶液的体积为 mL,用上述四种仪器中的某种测量某液体的体积,平视时读数为NmL,仰视时读数为MmL,若M>N,则所使用的仪器是 (填字母标号)。
(2)该滴定实验滴定终点的现象是 。
(3)步骤二中滴定操作图示(上右图)正确的是 (填编号)。
(4)步骤二的滴定过程温度变化并不明显,但操作过程中发现前一阶段溶液褪色较慢,中间阶段褪色明显变快,最后阶段褪色又变慢。试根据影响化学反应速率的条件分析,溶液褪色中间明显变快,最后又变慢的原因是 。
(5)请写出步骤三的操作内容 。
(6)若m的数值为1.340g,滴定的KMnO4溶液平均用量为25.00mL,则KMnO4溶液的浓度为 mol/L。
(7)若滴定完毕后读数时俯视,则实验误差为 (填“偏高”、“偏低”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烷烃的相对分子质量为30,请回答以下问题:
(1)该烷烃的结构简式为_________________;
(2)该烷烃与氯气在光照条件下生成一氯代物,请写出该反应的化学方程式___________________,该反应的反应类型为_______________;
(3)该烷烃可以由含有相同碳原子数的烯烃与氢气反应得到,请写出该反应的化学反应方程式
______________________,该反应的反应类型为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对可逆反应A(s)+3B(g) ![]() C(g)+2D(g) ΔH<0,在一定条件下达到平衡,下列有关叙述正确的是
C(g)+2D(g) ΔH<0,在一定条件下达到平衡,下列有关叙述正确的是
①增加A的量,平衡向正反应方向移动
②升高温度,平衡向逆反应方向移动,v(正)减小
③压强增大一倍,平衡不移动,v(正)、v(逆)不变
④增大B的浓度,v(正)>v(逆)
⑤加入催化剂,B的转化率提高
A.①② B.④ C.③ D.④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了测定中和反应的反应热,计算时至少需要的数据是( )
①酸的浓度和体积 ②碱的浓度和体积 ③比热容④反应后溶液的质量
⑤生成水的物质的量 ⑥反应前后溶液温度变化 ⑦操作所需的时间
A. ①②③⑥ B. ①③④⑥ C. ③④⑤⑥ D. 全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏伽德罗常数的值,下列说法正确的是
A. 20gD2O中含有的中子数为8NA
B. 3.36LNO2 与足量的水充分反应后,生成0.05NA 个NO 分子
C. 1mol 碳酸钠和碳酸氢钠的混合物中碳酸根离子的数目为NA
D. 3mol 单质Fe 完全燃烧转变为Fe3O4,失去8NA 个电子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com