
NA表示阿伏加德罗常数的值,常温下,抽去下图所示装置中的玻璃片,使两种气体充分反应。下列说法正确的是

A.反应前气体的总体积为1.344L
B.装置中产生大量的白色烟雾
C.反应前后分子总数不变,均为0.06 NA个
D.生成物充分溶于水后所得溶液含有0.01 NA个NH4+
科目:高中化学 来源:2014-2015江西省高二上学期期末化学试卷(解析版) 题型:实验题
(11分)某化学兴趣小组用如图所示装置电解CuSO4溶液,测定铜的相对原子质量。

(1)若实验中测定在标准状况下放出的氧气的体积VL,B连接直流电源的_________(填“正极”或“负极”);
(2)电解开始一段时间后,在U形管中可观察到的现象有__________________,电解的离子方程式为___________________________________。
(3)实验中还需测定的数据是_______________(填写序号)
①B极的质量增重m g
②A极的质量增重m g
(4)下列实验操作中必要的是________(填字母)
A.称量电解前电极的质量
B.电解后,取出电极直接烘干称重
C.刮下电解过程中电极上析出的铜,并清洗、称重
D.在有空气存在的情况下,烘干电极必须采用低温烘干的方法
(5)铜的相对原子质量为:___________(用含有m、V的计算式表示)
(6)如果用碱性(KOH为电解质)甲醇燃料电池作为电源进行实验,放电时负极电极反应式为___________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省高三3月阶段测试理综化学试卷(解析版) 题型:填空题
(14分)甲醇是一种重要的化工原料,在生产中有着重要的应用。工业上用天然气为原料,分为两阶段制备甲醇:
(i)制备合成气:CH4(g)+H2O(g) CO(g)+3H2(g)
CO(g)+3H2(g) 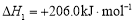
(ii)合成甲醇:CO(g)+2H2(g) CH3OH(g)
CH3OH(g) 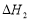
请回答下列问题:
(1)制备合成气:将1.0mol CH4和2.0mol H2O(g)通入反应室(容积为100L),在一定条件下发生反应(i);CH4的平衡转化率与温度、压强的关系如图所示。
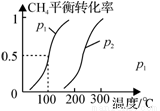
①已知100℃时达到平衡的时间为5min,则从反应开始到平衡,用氢气表示的平均反应速率为:v(H2) = 。
②图中p1 p2(填“<”、”“>”或“=”)。
③为解决合成气中H2过量而CO不足的问题,原料气中需添加CO2,发生反应如下:
CO2(g)+H2(g) CO(g)+H2O(g),为了使合成气配比最佳,理论上原料气中甲烷与二氧化碳体积比为 。
CO(g)+H2O(g),为了使合成气配比最佳,理论上原料气中甲烷与二氧化碳体积比为 。
(2)合成甲醇:在Cu2O/ZnO作催化剂的条件下,向2L的密闭容器中通入1mol CO(g)和2mol H2(g),发生反应(ii),反应过程中,CH3OH的物质的量(n)与时间(t)及温度的关系如图所示。
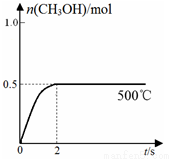
①反应(ii)需在 (填“高温”或“低温”)才能自发进行。
②据研究,反应过程中起催化作用的为Cu2O,反应体系中含少量的CO2 有利于维持Cu2O的量不变,
原因是 (用化学方程式表示)。
③在500℃恒压条件下,请在上图中画出反应体系中n(CH3OH)随时间t变化的总趋势图。
(3)工业上可通过甲醇羰基化法制取甲酸甲酯,其反应的热化学方程式为:
CH3OH(g)+CO(g) HCOOCH3(g)
HCOOCH3(g) 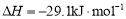 ,科研人员对该反应进行了研究,部分研究结果如下:
,科研人员对该反应进行了研究,部分研究结果如下:
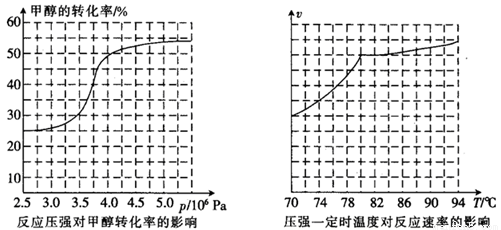
①从反应压强对甲醇转化率的影响“效率”看,工业制取甲酸甲酯应选择的压强是 。 (填“3.5×106Pa”、“4.0×106Pa”或“5.0×106Pa”)。
②实际工业生产中采用的温度是80℃,其理由是 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省温州市高三一模理综化学试卷(解析版) 题型:选择题
下列说法正确的是
A.还原性染料靛蓝的结构简式为: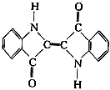 ,它的分子式是:C16H10N2O2
,它的分子式是:C16H10N2O2
B.结构为…-CH=CH-CH=CH-CH=CH-CH=CH-…的高分子化合物,其单体是乙烯
C.总质量一定时,乙炔和乙醛无论按什么比例混合,完全燃烧消耗氧气量或生成CO2量不变
D.丙烯酸(CH2=CHCOOH)和山梨酸(CH3CH=CHCH=CHCOOH)不是同系物,它们与氢气充分反应后的产物也不是同系物
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北省大冶市高三上学期期末联考理综化学试卷(解析版) 题型:填空题
(15分)研究碳及其化合物有重要意义。
(1)科学家用CO2和H2生产甲醇做燃料。
已知:甲醇的燃烧热ΔH= -726.5kJ/mol;氢气的燃烧热ΔH= -285.8kJ/mol;
则常温常压下,CO2(g)和H2(g)反应生成CH3OH(l)的热化学方程式 。
(2)460℃时,在4L密闭容器中充入1mol CO2和3.25mol H2,在一定条件下反应,测得CO2和CH3OH(g)的物质的量随时间的变化关系如图所示。
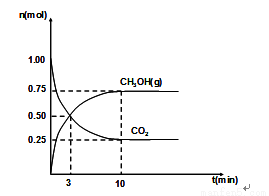
①从反应开始到3min时,H2O(g)的平均反应速率 ,
②下列措施中既能加快反应速率又能使H2的转化率增大的是 ,
A、使用更有效的催化剂
B、在原容器中再充入1mol CO2
C、在原容器中再充入1mol He
D、缩小容器的体积
E、将甲醇及时分离出来
③若该反应的焓变为ΔH,则下列示意图正确且能说明反应达到平衡状态的是________。
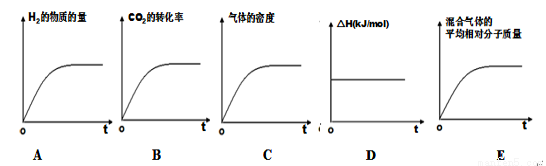
④该条件下,此反应的化学平衡常数为 。
(3)科学家研究发现,还可以用电催化法将CO2还原为碳氢化合物。原理如下图所示(电解质溶液是一种钾盐)。若CxHy为C2H4,则该原理的总反应式为为: 。
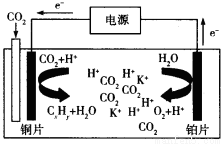
(4)已知
化学式 | 电离平衡常数 |
HCN | K=4.9×10-10 |
H2CO3 | K1=4.3×10-7、K2=5.6×10-11 |
①25℃时,测得HCN和NaCN的混合溶液的pH=11,则c(HCN)/c(CN-)=_________。
②向NaCN溶液中通入少量CO2,则发生反应的离子方程式为:________________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省高三下学期第一次月考理科综合化学试卷(解析版) 题型:填空题
(15分)α,β不饱和化合物在有机合成中有着广泛的用途。反应①是合成α,β不饱和化合物的常见的方法。
反应①:
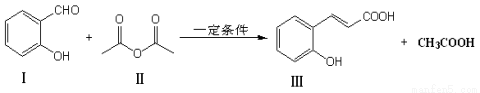
(1)化合物Ⅰ的分子式为 ,1mol化合物Ⅰ最多能与 molH2发生加成反应。
(2)下列说法,正确的是 。
A.反应①属于加成反应
B.化合物Ⅰ遇氯化铁溶液显紫色
C.化合物Ⅰ能与NaHCO3反应
D.化合物Ⅲ与Br2既能发生取代反应,也能发生加成反应
(3)化合物Ⅳ可以通过化合物Ⅲ在一定条件下发生分子内的酯化得到;请写出该反应的化学方程式(注明必要的条件) ,化合物Ⅴ是化合物Ⅳ的同分异构体,也是具有两个六元环的酯。化合物Ⅴ的结构简式为 。
(4)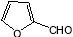 也能与化合物Ⅱ发生类似反应①的反应,除CH3COOH外,另一种有机产物的结构简式为 。在工业上化合物Ⅱ可以通过CH3CHO制备,请仅以乙烯为有机物原料两步合成CH3CHO,涉及的反应方程式为(注明必要的条件)① ;② 。
也能与化合物Ⅱ发生类似反应①的反应,除CH3COOH外,另一种有机产物的结构简式为 。在工业上化合物Ⅱ可以通过CH3CHO制备,请仅以乙烯为有机物原料两步合成CH3CHO,涉及的反应方程式为(注明必要的条件)① ;② 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省高三下学期第一次月考理科综合化学试卷(解析版) 题型:选择题
一种新型的乙醇电池,它用磺酸类质子溶剂。电池总反应为:C2H5OH +3O2 → 2CO2 +3H2O,电池示意如图,下列说法正确的是
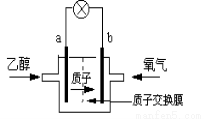
A.a极为电池的正极
B.电池工作时电流由a极沿导线经灯泡再到b极
C.电池负极的电极反应为:4H+ + O2 + 4e- = 2H2O
D.电池工作时,1mol乙醇被氧化时就有12mol电子转移
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省兰州市高三下学期诊断考试理综化学试卷(解析版) 题型:选择题
化学与人类生活、社会可持续发展密切相关。下列有关叙述中不正确的是
A.“海水淡化”可以解决“淡水供应危机”,加入明矾可以使海水淡化
B.采用加热方法消毒的目的是使蛋白质变性而杀灭细菌
C.含有重金属的电器废品不能随意丢弃,要分类回收并利用
D.煤炭燃烧过程中安装“固硫”装置,主要是为了减少二氧化硫的排放
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省深圳市南山区上学期高一化学期末试卷(解析版) 题型:选择题
在含1mol KAl(SO4)2的溶液中逐滴加入含2mol Ba(OH)2的溶液,下列说法中正确的是
A.先生成沉淀,后沉淀全部溶解
B.当溶液中Al3+全部沉淀出来时,沉淀的总物质的量最大
C.最后得到的沉淀是BaSO4
D.最后的沉淀为2mol BaSO4、1mol Al(OH)3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com