
 C(s)��H2O(g)����H��0�Ļ�ѧ��Ӧ����(v)��ʱ��(t)�Ĺ�ϵ��ͼ����ʾ���ǿ��淴Ӧ2NO2(g)
C(s)��H2O(g)����H��0�Ļ�ѧ��Ӧ����(v)��ʱ��(t)�Ĺ�ϵ��ͼ����ʾ���ǿ��淴Ӧ2NO2(g) N2O4(g)��H��0��Ũ��(c)��ʱ��(t)�ı仯���������˵����ȷ����
N2O4(g)��H��0��Ũ��(c)��ʱ��(t)�ı仯���������˵����ȷ����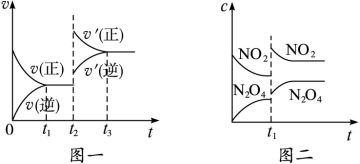
| A��ͼһ��t2ʱ�̺ͺ�ͼ����t1ʱ�̸ı���������п������������¶Ȼ�������ѹǿ |
| B����ͼ��t1ʱ�ı������������ѹǿ�����������ƽ����Է�����������С |
| C��ͼһ��ʾ���������´ﵽƽ��ʱ,v��(��)��v��(��)��ͼ����ʾ���������´ﵽƽ��ʱ,v��(��)��v��(��) |
| D��������������,�ֱ�ʹ�ò�ͬ����������Ӧ��ƽ�ⳣ�������� |

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 2NH3��g�� ��H=��92.4 kJ/mol
2NH3��g�� ��H=��92.4 kJ/mol| A��NH3���ɵ�������NH3�ֽ��������� |
B���������ķ�Ӧ���� v����NH3��=v����H2�� v����NH3��=v����H2�� |
| C�������ڵ��ܶȲ��ٱ仯 |
| D����λʱ��������a mol N2��ͬʱ����2a mol NH3 |
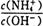 ֵ��_____(����� ����С�� ���䡱)��
ֵ��_____(����� ����С�� ���䡱)���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 H2+CO2���������ڼ���1molCO��1mol H2O��g��ʱ������2/3mol CO2���ͨ���H2O��g����Ϊ4molʱ�������������£�����CO2�����ʵ���Ϊ
H2+CO2���������ڼ���1molCO��1mol H2O��g��ʱ������2/3mol CO2���ͨ���H2O��g����Ϊ4molʱ�������������£�����CO2�����ʵ���Ϊ| A��0��5mol | B��0��6mol | C��0��9mol | D��2��5mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�������
 2NH3(g) ��H=��94.4kJ��mol��1������ʱ����ϵ�и�����Ũ����ʱ��仯��������ͼʾ��
2NH3(g) ��H=��94.4kJ��mol��1������ʱ����ϵ�и�����Ũ����ʱ��仯��������ͼʾ��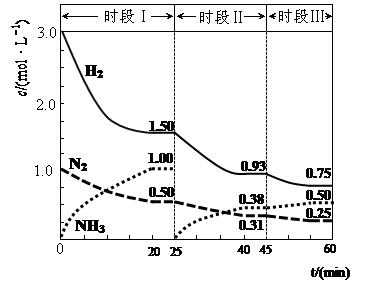
 5N2(g)+6H2O(g) ��H<0������Ӧ�ڣ�2NH3(g)+8NO(g)
5N2(g)+6H2O(g) ��H<0������Ӧ�ڣ�2NH3(g)+8NO(g) 5N2O(g)+3H2O(g) ��H��0��ƽ��������N2��N2O�������¶ȵĹ�ϵ����ͼ����ش���400K��600Kʱ��ƽ��������N2�������¶ȵı仯������ ���������ֹ��ɵ�ԭ���� ���δ������һ��ԭ��
5N2O(g)+3H2O(g) ��H��0��ƽ��������N2��N2O�������¶ȵĹ�ϵ����ͼ����ش���400K��600Kʱ��ƽ��������N2�������¶ȵı仯������ ���������ֹ��ɵ�ԭ���� ���δ������һ��ԭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 Ni(CO)4��g������֪�÷�Ӧƽ�ⳣ�����¶ȵĹ�ϵ���±���
Ni(CO)4��g������֪�÷�Ӧƽ�ⳣ�����¶ȵĹ�ϵ���±���
| A����������Ni(CO)4��g���ķ�ӦΪ���ȷ�Ӧ |
B��25��ʱ��ӦNi(CO)4(g)  Ni(s)+4CO��g����ƽ�ⳣ��Ϊ0.5(mol��L-1)3 Ni(s)+4CO��g����ƽ�ⳣ��Ϊ0.5(mol��L-1)3 |
| C����ij�����´ﵽƽ�⣬���Ni(CO)4��COŨ�Ⱦ�Ϊ0.5mol/L�����ʱ�¶ȸ���80�� |
| D��80��ﵽƽ��ʱ������������䣬����ϵ�г���һ������CO���ٴδﵽƽ���CO�����������С |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2C��g������2 s ����C��Ũ��Ϊ0.6 mol/L�����м���˵����ȷ���ǣ���������A��ʾ�ķ�Ӧ��ƽ������Ϊ0.3 mol/��L��s������������B��ʾ�ķ�Ӧ��ƽ������Ϊ0.6 mol/��L��s�����۷�Ӧ�ﵽƽ��ʱ��A��B��C�ķ�Ӧ����һ����ȣ��ܷ�Ӧ�ﵽƽ��ʱ��A��B��C�����ʵ��������ٱ仯
2C��g������2 s ����C��Ũ��Ϊ0.6 mol/L�����м���˵����ȷ���ǣ���������A��ʾ�ķ�Ӧ��ƽ������Ϊ0.3 mol/��L��s������������B��ʾ�ķ�Ӧ��ƽ������Ϊ0.6 mol/��L��s�����۷�Ӧ�ﵽƽ��ʱ��A��B��C�ķ�Ӧ����һ����ȣ��ܷ�Ӧ�ﵽƽ��ʱ��A��B��C�����ʵ��������ٱ仯�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 3C(g) �� D(s)����Ӧ�ﵽƽ��ʱC��Ũ��Ϊ1.2 mol/L.
3C(g) �� D(s)����Ӧ�ﵽƽ��ʱC��Ũ��Ϊ1.2 mol/L.�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 2SO3(g)��
2SO3(g)�� Fe3O4(g)��4H2(g)������м���SO2��O2��SO3�����ʵ����ֱ�Ϊx mol��3.25mol��1mol���Ҳ��м���9 mol��ˮ���������������ۣ��������۶����������Ӱ�죩��
Fe3O4(g)��4H2(g)������м���SO2��O2��SO3�����ʵ����ֱ�Ϊx mol��3.25mol��1mol���Ҳ��м���9 mol��ˮ���������������ۣ��������۶����������Ӱ�죩��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
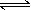 cC(g)����H="Q" kJ/mol��ͼ��ʾ����������¶ȡ�ѹǿ���ı仯��������Ӧ��Ӱ�졣�����ж���ȷ���ǣ�������
cC(g)����H="Q" kJ/mol��ͼ��ʾ����������¶ȡ�ѹǿ���ı仯��������Ӧ��Ӱ�졣�����ж���ȷ���ǣ�������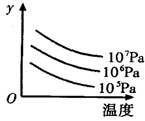
| A��a+b<cʱ��y���ʾƽ��������C���������� |
| B��a+b>cʱ��y���ʾƽ��������ƽ��Ħ������ |
| C��Q > 0ʱ��y���ʾ�ﵽƽ��ʱB��ת���� |
| D��Q < 0ʱ��y���ʾ�ﵽƽ��ʱA��Ũ�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com