
| A.新制的氯水在光照条件下颜色变浅 |
| B.H2、I2、HI平衡混合气加压后颜色变深 |
| C.KI溶液加氯水振荡后颜色变深 |
| D.加入催化剂有利于氨氧化的反应 |
科目:高中化学 来源:不详 题型:单选题
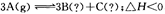 ,下列分析一定正确的是
,下列分析一定正确的是查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
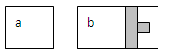
| A.a>b | B.a<b | C.a=b | D.无法确定 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 CO2(g)+H2 (g) △H<0
CO2(g)+H2 (g) △H<0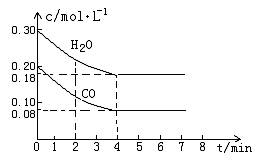
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
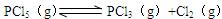 其中物质PCl3的物质的量变化如右图所示。
其中物质PCl3的物质的量变化如右图所示。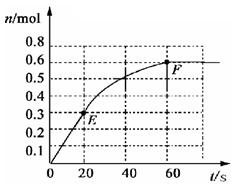
 )前 20
)前 20 s内 PCl5(g)的平均反应速率为
s内 PCl5(g)的平均反应速率为 查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
 2NH3(g),达平衡时NH3的浓度为4mol/L。请回答下列问题:
2NH3(g),达平衡时NH3的浓度为4mol/L。请回答下列问题:查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.在任何溶液中,c(Ca2+)、c(SO42-)均相等 |
B.b点将有沉淀生成,平衡后 溶液中c(SO42-)一定等于3´10-3 mol·L—1 溶液中c(SO42-)一定等于3´10-3 mol·L—1 |
| C.a点对应的Ksp等于c点对应的Ksp |
| D.d点溶液通过蒸发可以变到c点 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.35% | B.30% | C.1/4 | D.1/5 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
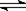 4C(g) + 6D(g) △H =-Q kJ/mol,在一定温度下达到化学平衡状态时,下列说法正确的是:( )
4C(g) + 6D(g) △H =-Q kJ/mol,在一定温度下达到化学平衡状态时,下列说法正确的是:( )查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com