
| A、乙二醇可用来生产聚酯纤维和作汽车发动机的抗冻剂 |
| B、乙醇是可再生能源,应大力推广“乙醇汽油”,含酒精的饮料中含有浓度不等的乙醇,75%(质量分数)的乙醇溶液常用于医疗消毒 |
| C、煤中含有煤焦油及多种化工原料,可通过煤的气化获得 |
D、据环保部门调查,2013年末,造成杭州自来水异味的元凶为邻叔丁基苯酚: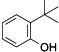 ,饮用含有该物质的水,对人体健康无任何不利影响 ,饮用含有该物质的水,对人体健康无任何不利影响 |
 的自来水会影响人体健康,故D错误.
的自来水会影响人体健康,故D错误.

科目:高中化学 来源: 题型:
| A、氢气是二次能源 |
| B、煤、石油、天然气均为化石能源 |
| C、只有农业废弃物、水生植物、油料植物中蕴含着丰富的生物质能 |
| D、太阳能是不可再生资源 |
查看答案和解析>>
科目:高中化学 来源: 题型:
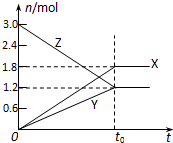 在一定温度下,将一定量的气体通入体积为2L的密闭容器中,使其发生反应,t0时容器中达到化学平衡,有关物质X、Y、Z的物质的量的变化如图所示.则下列有关推断正确的是( )
在一定温度下,将一定量的气体通入体积为2L的密闭容器中,使其发生反应,t0时容器中达到化学平衡,有关物质X、Y、Z的物质的量的变化如图所示.则下列有关推断正确的是( )| A、该反应的化学方程式为:3Z?3X+2Y |
| B、达到平衡时,X、Y、Z的质量不再改变 |
| C、达到平衡时,Z的浓度为1.2mol/L |
| D、达到平衡后,反应停止,反应速率为0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、大于3.2 g |
| B、等于3.2 g |
| C、小于3.2 g |
| D、任意质量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、高聚物脲醛树脂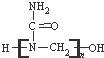 的合成单体之一是CH3OH 的合成单体之一是CH3OH |
B、按系统命名法,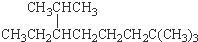 的名称为2,7,7-三甲基-3-乙基辛烷 的名称为2,7,7-三甲基-3-乙基辛烷 |
| C、有一种信息素的结构简式为CH3(CH2)5CH═CH(CH2)9CHO,为验证该物质中既含有醛基又含有碳碳双键,向该物质的试液中先加溴的CCl4溶液,观察到溶液褪色,继续滴加直到溶液变为红棕色,再向溶液中加入0.5mL H2O,充分振荡,观察到溶液褪色 |
D、化合物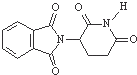 的分子式为C13H8O4N2 的分子式为C13H8O4N2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、除去SO42-最合适的试剂是BaCl2 |
| B、工业上通过电解氯化钠溶液制备金属钠和氯气 |
| C、室温下,AgCl在水中的溶解度大于在食盐水中的溶解度 |
| D、用酚酞试液可鉴别饱和食盐水和饱和纯碱溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
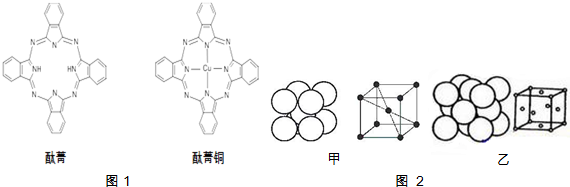
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com