

分析 (1)Cu原子失去4s能级1个电子形成亚铜离子;
(2)Cu晶体的堆积方式是面心立方最密堆积,配位数为12;
(3)往硫酸铜溶液中加入过量氨水,可生成[Cu(NH3)4]SO4,为配合物,其中Cu2+提供空轨道,NH3提供孤电子对;
(4)根据碳原子的成键情况要以判断碳原子的杂化方式;分子中含有2个π键,其它为σ键;
(5)SiO44-中价层电子对个数是4且不含孤电子对,利用均摊法计算其原子个数比,从而确定其化学式.
解答 解:(1)Cu原子失去4s能级1个电子形成亚铜离子,基态时亚铜离子核外电子排布式为为:1s22s22p63s23p63d10或[Ar]3d10,
故答案为:1s22s22p63s23p63d10或[Ar]3d10;
(2)Cu晶体的堆积方式是面心立方最密堆积,在金属晶体的最密堆积中,对于每个原子来说,在其周围的原子有与之同一层上有六个原子和上一层的三个及下一层的三个,故每个原子周围都有12个原子与之相连,
故答案为:面心立方最密堆积(或A1);12;
(3)A.[Cu(NH3)4]SO4为离子化合物,含有离子键,存在N-H极性键以及Cu-N配位键,故A正确;
B.在[Cu(NH3)4]2+中Cu2+提供空轨道,NH3提供孤电子对,故B错误;
C.[Cu(NH3)4]SO4组成元素中第一电离能最大的是N元素,最外层为半充满状态,故C错误;
D.SO42-与PO43- 互为等电子体,结构相似,中心原子形成4个σ键,空间构型均为正四面体,故D正确.
故答案为:A D;
(4)氨基乙酸铜的分子中存在C=O键,碳的杂化方式为sp2杂化,含有饱和碳原子,碳的杂化方式为sp3杂化;分子中含有4个N-H键、4个C-H键,2个C-N键、2个C-C键、2个C-O键,2个0-Cu键,以及2个C=O键,则共含有18个σ键,2个π键,该分子中σ键与π键个数比值为9:1,
故答案为:sp2、sp3;9:1;
(5)根据图片知,每个三角锥结构中Si原子是1个,O原子个数=2+2×$\frac{1}{2}$=3,所以硅原子和氧原子个数之比=1:3,3个O原子带6个单位负电荷,每个硅原子带4个单位正电荷,所以形成离子为[SiO3]n2n- (或SiO32-),故答案为:1:3;SiO32-(或(SiO3)n2n-.
点评 本题考查物质结构和性质,为高频考点,涉及配合物的成键情况、共价键、微粒空间构型判断、晶体类型判断等知识点,会利用价层电子对互斥理论判断原子杂化及微粒空间构型、会利用均摊法确定化学式等,难点是(5)题,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 向NH4HCO3溶液中加过量NaOH溶液并加热:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O | |
| B. | Fe3+溶液中滴加过量的氨水:Fe3++3OH-=Fe(OH)3↓ | |
| C. | 等体积等物质的量浓度的NaHCO3和Ba(OH)2溶液混合:HCO3-+Ba2++OH-═BaCO3↓+H20 | |
| D. | NaHCO3的水解:HCO3-+H2O=CO32-+H3O+ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 目前,汽车厂商常利用催化技术将尾气中的NO和CO转化成CO2和N2,化学方程式如下:2NO+2CO$\stackrel{催化剂}{?}$2CO2+N2.为研究如何提高该转化过程反应速率,某课题组进行了以下实验探究.
目前,汽车厂商常利用催化技术将尾气中的NO和CO转化成CO2和N2,化学方程式如下:2NO+2CO$\stackrel{催化剂}{?}$2CO2+N2.为研究如何提高该转化过程反应速率,某课题组进行了以下实验探究.| 实验编号 | 实验目的 | T/℃ | NO初始浓度 mol/L | CO初始浓度 mol/L | 同种催化剂的比表面积m2/g |
| Ⅰ | 为以下实验作参照 | 280 | 6.50×10-3 | 4.00×10-3 | 80 |
| Ⅱ | 探究催化剂比表面积对尾气转化速率的影响 | 280 | 6.50×10-3 | 4.00×10-3 | 120 |
| Ⅲ | 探究温度对尾气转化速率的影响 | 360 | 6.50×10-3 | 4.00×10-3 | 80 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
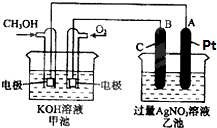 请按要求回答下列问题:
请按要求回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | X、Y、Z元素分别为N、P、O | |
| B. | 白格中都是主族元素,灰格中都是副族元素 | |
| C. | 原子半径:Z>X>Y | |
| D. | X、Y、Z的气态氢化物中最稳定的是:X的氢化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某研究小组探究将废塑料隔绝空气加强热使其变成有用的物质,实验装置如图.
某研究小组探究将废塑料隔绝空气加强热使其变成有用的物质,实验装置如图.| 产物 | 氢气 | 甲烷 | 乙烯 | 丙烯 | 苯 | 甲苯 | 碳 |
| 质量分数(%) | 12 | 24 | 12 | 16 | 20 | 10 | 6 |
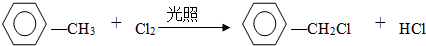 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
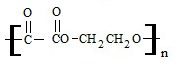 +2nH2O.
+2nH2O.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com