
| a | |||||||
| b | c | d | |||||
| e | f | g |
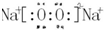 ;b、g元素形成的bg2作为溶剂可溶解S单质(填写该单质“名称”或“化学式”)
;b、g元素形成的bg2作为溶剂可溶解S单质(填写该单质“名称”或“化学式”) 分析 由元素在周期表中位置可知,a为H、b为C、c为N、d为O、e为Na、f为Al、g为S,
(1)电子层结构相同的离子,核电荷数越大离子半径越小;
(2)同周期自左而右元素非金属性增强,可以利用最高价含氧酸中强酸制备弱酸进行验证;
(3)d、e元素形成的四原子化合物为Na2O2;b、g元素形成的分子为SC2,可溶解S单质.
解答 解:由元素在周期表中位置可知,a为H、b为C、c为N、d为O、e为Na、f为Al、g为S,
(1)电子层结构相同的离子,核电荷数越大离子半径越小,故离子半径:O2->Na+,
故答案为:O2-;Na+;
(2)同周期自左而右元素非金属性增强,故非金属性N>C,可以利用最高价含氧酸中强酸制备弱酸进行验证,反应方程式为:2HNO3+Na2CO3 =2NaNO3+CO2↑+H2O,
故答案为:N;2HNO3+Na2CO3 =2NaNO3+CO2↑+H2O;
(3)d、e元素形成的四原子化合物为Na2O2,电子式为: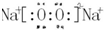 ,b、g元素形成的分子SC2为直线型对称结构,分子中正负电荷重心重合,属于非极性溶剂,可溶解S单质,
,b、g元素形成的分子SC2为直线型对称结构,分子中正负电荷重心重合,属于非极性溶剂,可溶解S单质,
故答案为: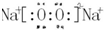 ;S.
;S.
点评 本题考查了原子结构与元素周期律的综合应用,题目难度中等,明确原子结构与元素周期表的关系为解答关键,注意熟练掌握元素周期律的内容,试题培养了学生的分析能力及灵活应用能力.


 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源: 题型:解答题
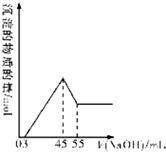 准确称取10.0g铝土矿样品(含Al2O3、Fe2O3、SiO2),加入100mL硫酸溶液,充分反应后向滤液中加入10mol/L的NaOH溶液,产生沉淀的物质的量与加入NaOH溶液的体积关系如图所示:
准确称取10.0g铝土矿样品(含Al2O3、Fe2O3、SiO2),加入100mL硫酸溶液,充分反应后向滤液中加入10mol/L的NaOH溶液,产生沉淀的物质的量与加入NaOH溶液的体积关系如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 洗涤的目的一般是除去沉淀或晶体表面可溶性的杂质,提高纯度 | |
| B. | 洗涤的试剂一般可选用蒸馏水、冰水、乙醇、该物质的饱和溶液 | |
| C. | 洗涤的操作是向过滤器里的固体加洗涤剂,使洗涤剂浸没固体,待洗涤剂自然流下 | |
| D. | 洗净的检验是检验最后一次洗涤液中是否含有形成沉淀的该溶液中的离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 实验序号 | 实验内容 | 实验结果 |
| a | 加AgNO3溶液 | 有白色沉淀生成 |
| b | 加足量NaOH溶液并加热 | 收集到气体1.12 L(已折算成标准状况下的体积) |
| c | 加足量BaCl2溶液时,对所得沉淀进行洗涤、干燥、称量;再向沉淀中加足量稀盐酸,然后干燥、称量 | 第一次称量读数为6.27 g,第二次称量读数为2.33 g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl2具有很强的氧化性,在化学反应中只能作氧化剂 | |
| B. | Cl-、Cl为不同的核素,有不同的化学性质 | |
| C. | 实验室制备Cl2,可用排饱和食盐水集气法收集 | |
| D. | 电解饱和食盐水制氯气时,与电源负极相连的石墨棒上方充满黄绿色气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 127I与131I互为同素异形体 | B. | 137Cs的核电荷数为137 | ||
| C. | 铀235的中子数是143 | D. | 铯与水的反应比钠与水的反应缓慢 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 离子组 | 分析 |
| A | 含大量Al3+的溶液中:K+、Na+、NO3-、CO32- | 不能大量共存,因有Al2(CO3)3沉淀生成 |
| B | 含大量Fe3+的溶液中:K+、Mg2+、I-、NO3- | 不能大量共存,因2Fe3++2I-=2Fe2++I2 |
| C | 由水电离的c(H+)=1×10-14mol/L的溶液中: Ca2+、NO3-、HCO3-、Cl- | 不能大量共存,因溶液呈酸性,与HCO3-反应产生CO2气体 |
| D | 使酚酞变红的溶液中: Na+、K+、SO32-、S2- | 不能大量共存,因SO32-和S2-反应产生淡黄色的S沉淀 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com