
 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:
 现有三个反应:
现有三个反应:| T/℃ | 700 | 800 |
| K1 | 2.38 | 2.56 |
| K2 | 0.80 |
| 反应时间/min | 0 | 2 | 4 | 6 |
| n(CO)/mol | 1.20 | 0.90 | 0.80 | |
| n(H2O)/mol | 0.60 | 0.20 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 离子或分子 | 要求 |
| A | K+、NO3-、Cl-、HS- | c(K+)<c(Cl-) |
| B | Fe3+、NO3-、SO32-、Cl- | 滴加盐酸立即有气体产生 |
| C | NH4+、Al3+、SO42-、CH3COOH | 滴加NaOH溶液立即有气体产生 |
| D | Na+、HCO3-、Mg2+、SO42- | 滴加氨水立即有沉淀产生 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
 现需配制0.1mol/LNaOH溶液480mL,如图是某同学转移溶液的示意图.
现需配制0.1mol/LNaOH溶液480mL,如图是某同学转移溶液的示意图.查看答案和解析>>
科目:高中化学 来源: 题型:
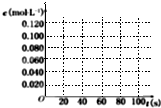 已知:N2O4(g)=2NO2(g);△H=+57.20kJ?mol-1.
已知:N2O4(g)=2NO2(g);△H=+57.20kJ?mol-1.| 时间(s) | 0 | 20 | 40 | 60 | 80 |
| c(N2O4)/mol/L | 0.100 | c1 | 0.050 | c3 | c4 |
| c(NO2)/mol/L | 0.000 | 0.060 | c2 | 0.120 | 0.120 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com