
【题目】下列溶液加热蒸干、灼烧后,能析出原溶质固体的是( )
A.AlCl3
B.KHCO3
C.Fe2(SO4)3
D.NH4HCO3
科目:高中化学 来源: 题型:
【题目】(1)在粗制CuSO4·5H2O晶体中常含有杂质Fe2+。在提纯时为了除去Fe2+,常加入合适氧化剂,使Fe2+氧化为Fe3+,下列物质可采用的是________
A. KMnO4 B. H2O2 C. Cl2 水 D. HNO3
然后再加入适当物质调整至溶液pH=3.8,使Fe3+转化为Fe(OH)3,可以达到除去Fe3+而不损失CuSO4的目的,调整溶液pH可选用下列中的________
A. NaOH B. NH3·H2O C. CuO D. Cu(OH)2
(2)甲同学怀疑调整至溶液pH=4是否能达到除去Fe3+而不损失Cu2+的目的,乙同学认为可以通过计算确定,已知lg2=0.3,常温下Fe(OH)3的溶度积Ksp=8.0×10-38,Cu(OH)2的溶度积Ksp=3.0×10-20,通常认为残留在溶液中的离子浓度小于1×10-5 mol·L-1时就认为沉淀完全,设溶液中CuSO4的浓度为3.0 mol·L-1,则Cu(OH)2开始沉淀时溶液的pH为____,Fe3+完全沉淀时溶液的pH为____,通过计算确定上述方案________(填“可行”或“不可行”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向体积为2L的固定密团容器中通入3molX气体,在一定温度下发生如下反应:2X(g) ![]() Y(g)+3Z(g)。
Y(g)+3Z(g)。
(1)经5min后反应达到平衡,容器内的压强为起始时的1.2倍,则Y的反应速率为________mol/(L·min)。
(2)若上述反应在甲、乙、丙、丁四个同样的密闭容器中进行,在同一段时间内测得容器内的反应速率分别为甲:v(X)=3.5 mol/(L·min);乙:v(Y)=2 mol/(L·min);丙:v(Z)=4.5 mol/(L·min);丁:v(X)=3.5 mol/(L·s)。若其他条件相同,温度不同,则温度由高到低的顺序是(填序号)______。
(3)向达到(1)所述的平衡体系中充入氦气,则平衡_______(填“向左”、“向右”或“不”) 移动;从(1)所述的平衡体系中移走部分Y气体,则平衡_______(填“向左”、“向右”或“不”) 移动。
(4)在相同条件下向达到(1)所述的平衡体系中再充入0.5molX气体,则平衡后X的转化率与(1)所述的平衡中X的转化率相比较_________。
A.无法确定 B.前者定大于后者 C.前者一定等于后者 D.前者一定小于后者
(5)保持温度和压强不变,起始时加入X、Y、Z物质的量分别为amol、bmol、cmol,a为任意值,达到平衡时仍与(1)的平衡等效。则:b、c该满足的关系为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某白色固体混合物由NaCl、KCl、MgSO4、CaCO3中的两种组成,进行如下实验:① 混合物溶于水,得到澄清透明溶液;② 做焰色反应,通过钴玻璃可观察到紫色;③ 向溶液中加碱,产生白色沉淀。根据实验现象可判断其组成为
A.KCl、NaClB.KCl、MgSO4
C.KCl、CaCO3D.MgSO4、NaCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列盐:①FeCl3 ②CH3COONa ③NaCl,其水溶液的pH由大到小排列正确的是( )
A.①>③>②
B.②>③>①
C.③>②>①
D.①>②>③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学反应能量变化的叙述中正确的是
A. 燃烧反应一定是放热反应
B. 只要是在点燃条件下进行的反应就一定是吸热反应
C. 只要是在常温常压下进行的反应就一定是放热反应
D. 如果反应物的总能量低于生成物的总能量,该反应一定是放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙二酸俗名草酸,易溶于水,其水溶液与酸性KMnO4溶液反应的离子方程式为:2MnO4﹣+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O
为了测定草酸晶体H2C2O4·xH2O中的x值,某实验小组进行实验,步骤如下:
①称取1.260g草酸晶体,配成100mL溶液。
②取25.00mL该H2C2O4溶液加入锥形瓶内,再加入适量稀硫酸。
③用浓度为0.1000mol/L的KMnO4标准溶液进行滴定,至滴定达到终点。
④重复实验。记录整理数据如下:
实验序号 | V(KMnO4溶液) | |
滴定前刻度/mL | 滴定后刻度/mL | |
1 | 0.10 | 10.00 |
2 | 1.10 | 11.10 |
3 | 1.50 | 13.50 |
4 | 0.70 | 10.80 |
回答下列问题:
(1)步骤①需要使用烧杯、量筒、玻璃棒、胶头滴管,还缺少的玻璃仪器为_______(填名称);步骤③滴定过程中,盛装KMnO4溶液的仪器为__________________(填名称)。
(2)本实验滴定达到终点的标志是__________________________;
(3)根据数据,计算H2C2O4溶液的物质的量浓度为______mol/L,x=____________;
(4)若滴定终点时俯视滴定管刻度,则x值会______(填“偏大”、“偏小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E均为有机物,其中A是化学实验中最常见的有机物,它易溶于水并有特殊香味;B的产量可衡量一个国家石油化工发展的水平,有关物魇的转化关系如图①所示: 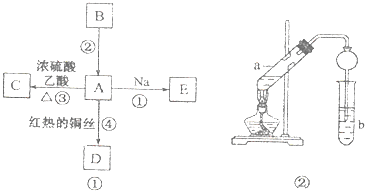
(1)A中官能团的名称为 .
(2)写出下列反应的化学方程式反应①;反应④;
(3)实验室利用反应③制取C,常用上图②装置: ①a试管中的主要化学反应的方程式为: .
②在实验中球形干燥管除起冷凝作用外,另一个重要作用是 .
③试管b中观察到的现象是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com