
1831ÄźĄī±ČĻ£Ģį³öĮĖČ·¶ØÓŠ»śĪļÖŠĒāŗĶĢ¼µÄÖŹĮæ·ÖŹżµÄ·½·Ø£¬Ę仳±¾ŌĄķŹĒŌŚøßĪĀĻĀŃõ»ÆÓŠ»śĪļ£¬ĘäÉś³ÉĪļÖ÷ŅŖŹĒ(””””)
A£®COŗĶH2O B£®COŗĶH2
C£®CO2ŗĶH2O D£®CO2ŗĶH2
 ĘŚÄ©1¾ķĖŲÖŹ½Ģӿʥ¹Ą¾ķĻµĮŠ“š°ø
ĘŚÄ©1¾ķĖŲÖŹ½Ģӿʥ¹Ą¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠĄė×Ó·½³ĢŹ½ÕżČ·µÄŹĒ £Ø £©
A£®MnO2 ÓėÅØŃĪĖį·“Ó¦ÖĘCl2£ŗMnO2+4HCl Mn2£«+2Cl£+Cl2”ü+2H2O
Mn2£«+2Cl£+Cl2”ü+2H2O
B£®Ė«ŃõĖ®¼ÓČėĻ”ĮņĖįŗĶKIČÜŅŗ£ŗH2O2£«2H£«£«2I£=I2£«2H2O
C£®Ca(HCO3)2ČÜŅŗÓėÉŁĮæNaOHČÜŅŗ·“Ó¦£ŗ2HCO3£ +Ca2£«+2OH£=CaCO3”ż+2H2O+CO32£
D£®Na2S2O3ČÜŅŗÖŠ¼ÓČėĻ”ĮņĖį£ŗ2S2O32££«4H£«=SO42££«3S”ż£«2H2O
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
°“·Ö×Ó½į¹¹¾ö¶ØŠŌÖŹµÄ¹ŪµćæÉĶʶĻ
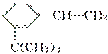 ÓŠČēĻĀŠŌÖŹ£ŗ
ÓŠČēĻĀŠŌÖŹ£ŗ
(1)±½»·²æ·ÖæÉ·¢Éś________·“Ó¦ŗĶ________·“Ó¦”£
(2)”ŖCH===CH2²æ·ÖæÉ·¢Éś________·“Ó¦ŗĶ________·“Ó¦”£
(3)øĆÓŠ»śĪļÖŠµĪČėäåĖ®ŗóÉś³É²śĪļµÄ½į¹¹¼ņŹ½ĪŖ______________________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĶ¼ŹĒŅ»ÖÖŠĪדæįĖĘŅ»ĢõŠ”¹·µÄÓŠ»śĪļ£¬»Æѧ¼ŅTim Rickard½«ĘäČ”ĆūĪŖ”°doggycene”±£¬ĻĀĮŠÓŠ¹ŲdoggyceneµÄĖµ·ØÕżČ·µÄŹĒ(””””)
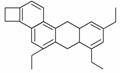
A£®”°doggycene”±ÖŠĖłÓŠĢ¼Ō×Ó²»æÉÄÜ“¦ÓŚĶ¬Ņ»Ę½ĆęÉĻ
B£®øĆĪļÖŹµÄ·Ö×ÓŹ½ĪŖC26H30
C£®³£ĪĀĻĀøĆÓŠ»śĪļĪŖĘųĢ¬
D£®1 moløĆĪļÖŹŌŚŃõĘųÖŠĶźČ«Č¼ÉÕÉś³ÉCO2ŗĶH2OµÄĪļÖŹµÄĮæÖ®±ČĪŖ2”Ć1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
¹¤ŅµÉĻ“Ó·ĻĒ¦Šīµē³ŲµÄĒ¦øą»ŲŹÕĒ¦µÄ¹ż³ĢÖŠ£¬æÉÓĆĢ¼ĖįŃĪČÜŅŗÓė“¦ĄķŗóµÄĒ¦øą(Ö÷ŅŖ³É·ÖĪŖPbSO4)·¢Éś·“Ó¦£ŗPbSO4(s)£«CO32£(aq) PbCO3(s)£«SO42£(aq)”£Ä³æĪĢā×éÓĆPbSO4ĪŖŌĮĻÄ£ÄāøĆ¹ż³Ģ£¬Ģ½¾æÉĻŹö·“Ó¦µÄŹµŃéĢõ¼ž¼°¹ĢĢå²śĪļµÄ³É·Ö”£
PbCO3(s)£«SO42£(aq)”£Ä³æĪĢā×éÓĆPbSO4ĪŖŌĮĻÄ£ÄāøĆ¹ż³Ģ£¬Ģ½¾æÉĻŹö·“Ó¦µÄŹµŃéĢõ¼ž¼°¹ĢĢå²śĪļµÄ³É·Ö”£
£Ø1£©ÉĻŹö·“Ó¦µÄĘ½ŗā³£Źż±ķ“ļŹ½£ŗK=
£Ø2£©ŹŅĪĀŹ±£¬ĻņĮ½·ŻĻąĶ¬µÄPbSO4ѳʷ֊·Ö±š¼ÓČėĶ¬Ģå»ż”¢Ķ¬ÅØ¶ČµÄNa2CO3ŗĶNaHCO3ČÜŅŗ¾łæÉŹµĻÖÉĻŹö×Ŗ»Æ”£ŌŚ ČÜŅŗÖŠPbSO4×Ŗ»ÆĀŹ½Ļ“ó£¬ĄķÓÉŹĒ
£Ø3£©²éŌÄĪÄĻ×£ŗÉĻŹö·“Ó¦»¹æÉÄÜÉś³É¼īŹ½Ģ¼ĖįĒ¦[2PbCO3·Pb(OH)2]£¬ĖüŗĶPbCO3ŹÜČȶ¼Ņ×·Ö½āÉś³ÉPbO”£øĆæĪĢā×é¶Ō¹ĢĢå²śĪļ£Ø²»æ¼ĀĒPbSO4£©µÄ³É·ÖĢį³öČēĻĀ¼ŁÉč”£ĒėÄćĶź³É¼ŁÉ趞ŗĶ¼ŁÉčČż£ŗ
¼ŁÉčŅ»£ŗČ«²æĪŖPbCO3£»
¼ŁÉ趞£ŗ £»
¼ŁÉčČż£ŗ ”£
£Ø4£©ĪŖŃéÖ¤¼ŁÉčŅ»ŹĒ·ń³ÉĮ¢£¬æĪĢā×é½ųŠŠČēĻĀŃŠ¾æ£ŗ
¢Ł¶ØŠŌŃŠ¾æ£ŗĒėÄćĶź³ÉĻĀ±ķÖŠÄŚČŻ
| ŹµŃé²½Öč(²»ŅŖĒ󊓳ö¾ßĢå²Ł×÷¹ż³Ģ£© | Ō¤ĘŚµÄŹµŃéĻÖĻóŗĶ½įĀŪ |
| Č”Ņ»¶ØĮæѳʷ³ä·ÖøÉŌļ£¬ |
¢Ś¶ØĮæŃŠ¾æ£ŗČ”26.7 mgµÄøÉŌļѳʷ£¬¼ÓČČ£¬²ā
µĆ¹ĢĢåÖŹĮæĖęĪĀ¶ČµÄ±ä»Æ¹ŲĻµČēĻĀĶ¼”£Ä³Ķ¬Ń§
ÓÉĶ¼ÖŠŠÅĻ¢µĆ³ö½įĀŪ£ŗ¼ŁÉčŅ»²»³ÉĮ¢”£ÄćŹĒ·ń
Ķ¬ŅāøĆĶ¬Ń§µÄ½įĀŪ£¬²¢¼ņŹöĄķÓÉ£ŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ijĢžÖŠĢ¼ŌŖĖŲŗĶĒāŌŖĖŲµÄÖŹĮæ±ČĪŖ24”Ć5£¬øĆĢžŌŚ±ź×¼×“æöĻĀµÄĆܶȏĒ2.59 g”¤L£1£¬ŌņĘä·Ö×ÓŹ½ĪŖ(””””)
A£®C2H6 B£®C4H10 C£®C5H8 D£®C7H8
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŅŅ“¼“ß»ÆŃõ»ÆĪŖŅŅČ©¹ż³ĢÖŠ»Æѧ¼üµÄ¶ĻĮŃÓėŠĪ³ÉĒéæöæɱķŹ¾ČēĻĀ£ŗ
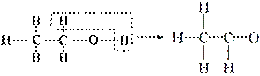
ĻĀĮŠ“¼Äܱ»Ńõ»ÆĪŖČ©Ąą»ÆŗĻĪļµÄŹĒ(””””)
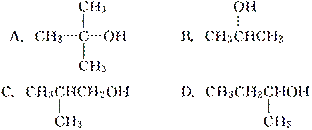
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
£Ø1£©»·¾³×ؼŅČĻĪŖæÉŅŌÓĆ½šŹōĀĮ½«Ė®ĢåÖŠµÄNO ×Ŗ»ÆĪŖN2£¬“Ó¶ųĒå³żĪŪČ¾”£øĆ·“Ó¦ÖŠÉę¼°µÄĮ£×ÓÓŠ£ŗH2O”¢Al”¢OH
×Ŗ»ÆĪŖN2£¬“Ó¶ųĒå³żĪŪČ¾”£øĆ·“Ó¦ÖŠÉę¼°µÄĮ£×ÓÓŠ£ŗH2O”¢Al”¢OH ”¢Al(OH)3”¢NO
”¢Al(OH)3”¢NO ”¢N2£¬Š“³ö·“Ó¦µÄĄė×Ó·½³ĢŹ½ ”£
”¢N2£¬Š“³ö·“Ó¦µÄĄė×Ó·½³ĢŹ½ ”£
£Ø2£©ĪŅ¹śŹ×““µÄŗ£Ńóµē³ŲŅŌŗ£Ė®ĪŖµē½āÖŹČÜŅŗ£¬µē³Ų×Ü·“Ó¦ĪŖ£ŗ4Al+3O2+6H2O=4Al(OH)3”£µē³ŲÕż¼«µÄµē¼«·“Ó¦Ź½ĪŖ ”£
£Ø3£©ŅŃÖŖ£ŗ¢Ł4Al(s)+3O2(g)=2Al2O3(g) ”÷H=£2834.9kJ/mol
¢ŚFe2O3(s)+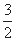 C(s)=
C(s)= 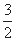 CO2(g)+2Fe(s) ”÷H=+234.1kJ/mol
CO2(g)+2Fe(s) ”÷H=+234.1kJ/mol
¢ŪC(s)+O2(g)=CO2(g) ”÷H=£393.5kJ/mol
Š“³öĀĮÓėŃõ»ÆĢś·¢ÉśĀĮČČ·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ ”£
£Ø4£©½«Ņ»¶ØÖŹĮæµÄÄĘĀĮŗĻ½šÖĆÓŚĖ®ÖŠ£¬ŗĻ½šČ«²æČܽā£¬µĆµ½20mol£¬pH=14µÄČÜŅŗ£¬Č»ŗó2mol/LŃĪĖįµĪ¶Ø£¬æÉµĆ³ĮµķÖŹĮæÓėĻūŗĵÄŃĪĖįĢå»ż¹ŲĻµČēĻĀĶ¼£ŗ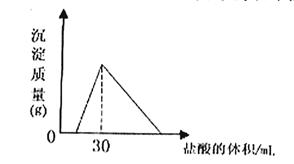 Ōņ·“Ó¦¹ż³ĢÖŠ²śÉśĒāĘųµÄ×ÜĢå»żĪŖ L£Ø±ź×¼×“æö£©
Ōņ·“Ó¦¹ż³ĢÖŠ²śÉśĒāĘųµÄ×ÜĢå»żĪŖ L£Ø±ź×¼×“æö£©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
.ŌŚĄė×ÓÅØ¶Č¶¼ĪŖ0.1 mol/LĻĀĮŠČÜŅŗÖŠ£¬¼ÓČė£Ø»ņĶØČė)ijĪļÖŹŗ󣬷¢Éś·“Ó¦ĻČŗóĖ³ŠņÕżČ·ŹĒ
A.ŌŚŗ¬Fe3+”¢ Cu2+”¢ H+µÄČÜŅŗÖŠ¼ÓČėŠæ·Ū£ŗCu 2+”¢ Fe3+”¢H+
B.ŌŚŗ¬I-”¢SO32£”¢Br-µÄČÜŅŗÖŠ²»¶ĻĶØČėĀČĘų:I-”¢Br-”¢SO32£
C.ŌŚŗ¬AlO2£”¢SO32£”¢OH£µÄČÜŅŗÖŠÖšµĪ¼ÓČėĮņĖįĒāÄĘČÜŅŗ:OH£”¢AlO2£”¢SO3£
D.ŌŚŗ¬Fe 3+”¢ H+”¢NH4+ µÄČÜŅŗÖŠÖš½„¼ÓČėÉÕ¼īČÜŅŗ:Fe3+”¢NH4+”¢H+
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com