
| A. | 属于钾盐 | B. | 属于碳酸盐 | C. | 属于正盐 | D. | 属于酸式盐 |
分析 对K2CO3分类,可以依据所含金属阳离子、酸根阴离子进行分类,也可以依据盐的组成分类,盐分为正盐、酸式盐、碱式盐、复盐、络盐等.酸和碱恰好完全反应生成的盐为正盐,多元酸被碱部分中和生成的盐为酸式盐,根据含有钾元素的盐为钾盐,含有碳酸根的盐为碳酸盐,依此分析.
解答 解:A.钾盐是指电离出钾离子和酸根阴离子的盐,碳酸钾符属于钾盐,故A正确;
B.碳酸盐是电离出金属阳离子和碳酸根离子的盐,碳酸钾,属于碳酸盐,故B正确;
C.K2CO3可以看做氢氧化钾和碳酸完全反应生成的盐,组成上分类为正盐,故C正确;
D.酸式盐是多元酸部分被碱中和反应生成的盐,K2CO3是正盐,不是酸式盐,故D错误;
故选D.
点评 本题考查化学基本概念、物质分类,涉及正盐、酸式盐、碳酸盐等,题目难度不大,注意对概念的理解.


 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案科目:高中化学 来源: 题型:多选题
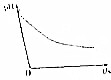 某离子反应涉及H2O、CLO-、NH4+、H+、N2、CL-六种微粒.常温条件下反应时,溶液pH随时间变化的曲线如图所示,下列判断错误的是( )
某离子反应涉及H2O、CLO-、NH4+、H+、N2、CL-六种微粒.常温条件下反应时,溶液pH随时间变化的曲线如图所示,下列判断错误的是( )| A. | 该反应的氧化剂是CLO- | |
| B. | 该反应中有两种离子生成 | |
| C. | 该反应生成1mol氧化产物时,转移的电子为6mol | |
| D. | 参加反应的氧化剂与还原剂的物质的量之比为2:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 56g Fe与稀HNO3完全反应时一定转移3NA个电子 | |
| B. | 标准状况下11.2 L NH3溶于1 L水中,溶液中含N原子的微粒总数为0.5NA | |
| C. | 常温常压下,0.1NA个Al与足量氢氧化钠溶液反应生成3.36 LH2 | |
| D. | 同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的△H不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、Cl-、HCO3-、Ca2+ | B. | OH-、Na+、Mg2+、HCO3- | ||
| C. | Na+、Cl-、H+、Ag+ | D. | Na+、SiO32-、H+、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
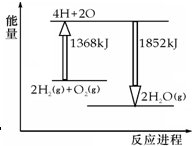
| A. | 拆开2molH2(g)和1molO2(g)中的化学键成为H、O原子,共吸收1368kJ能量 | |
| B. | 由H、O原子形成2molH2O(g),共放出1852kJ能量 | |
| C. | 2molH2(g)和1molO2(g)反应生成2molH2O(g),共吸收484kJ能量 | |
| D. | 2molH2(g)和1molO2(g)反应生成2molH2O(l),放出热量大于484kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
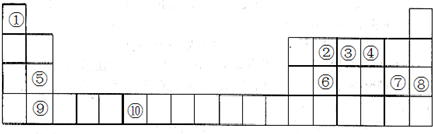
| A. | ①③ | B. | ②③ | C. | ②③⑤⑥ | D. | ①②③④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该溶液中水电离出的c(H+)=10-8mol/L | |
| B. | 加水稀释,醋酸钠的水解程度增大,水的电离程度也增大 | |
| C. | 加入盐酸,pH=7时,有c(C1-)=c(CH3COOH) | |
| D. | 向溶液中加入醋酸呈酸性,则一定是c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com