


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
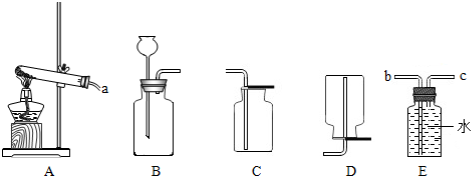
 有机物A在常温下为气体,标准状况下密度为1.25g/L;F为六元环状结构;又已知R-CHO
有机物A在常温下为气体,标准状况下密度为1.25g/L;F为六元环状结构;又已知R-CHO| 催化剂 |
| O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
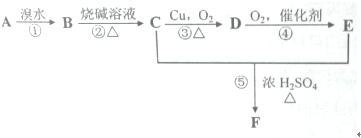
 已知:在常温下,浓度均为0.1mol?L-1的下列六种溶液的pH:
已知:在常温下,浓度均为0.1mol?L-1的下列六种溶液的pH:| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 11.3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| H2(g) | Br2(g) | HBr(g) | |
| 1mol分子中的化学键断裂时需要吸收的能量/kJ | 436 | a | 369 |
| A、230 | B、200 |
| C、404 | D、260 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com