
【题目】(NH4)2SO4在一定条件下发生如下反应:4(NH4)2SO4 = N2↑ + 6NH3↑ + 3SO2↑ + SO3↑ + 7H2O,将反应后的混合气体先通过浓硫酸,再通入足量的BaCl2溶液,结果为
A.产生BaSO3沉淀 B.产生BaSO4沉淀
C.产生BaSO4和BaSO3沉淀 D.无沉淀产生
科目:高中化学 来源: 题型:
【题目】高纯度氧化铝有广泛的用途,某研究小组用以下流程制取高纯度氧化铝:
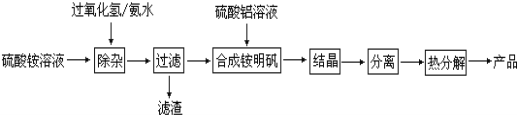
根据上述流程图填空:
(1)“除杂”操作是先加入过氧化氢充分反应后,再用氨水调节溶液的pH,使硫酸铵溶液中的少量Fe2+氧化为Fe3+并进一步转化为Fe(OH)3从而除去Fe2+,则Fe2+酸性条件下氧化为Fe3+的离子方程式为: 。
(2)配制硫酸铝溶液时,需用硫酸酸化,酸化的目的是 。
(3)“分离”操作的名称是 (填字母代号)。
A.蒸馏 B.分液 C.过滤
(4)铵明矾晶体的化学式为NH4Al(SO4)212H2O,铵明矾属于 (填“纯净物”或“混合物”)在0.1mol/L铵明矾的水溶液中,浓度最大的离子是 。
(5)热分解中发生如下反应6NH4Al(SO4)2 = 3Al2O3 + 2NH3 ↑+ 2N2 ↑+ 6SO2 ↑+ 6SO3 ↑+ 9H2O,当生成1mol Al2O3时转移电子物质的量为 mol;
(6)往含0.1mol铵明矾稀溶液中逐滴加入含0.3mol Ba(OH)2的稀溶液,反应的总离子方程式为: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列四支试管中,过氧化氢分解的化学反应速率最大的是( )
试管 | 温度 | 过氧化氢浓度 | 催化剂 |
A | 室温(25℃) | 12% | 有 |
B | 水浴加热(50℃) | 4% | 无 |
C | 水浴加热( 50℃) | 12% | 有 |
D | 室温(25℃) | 4% | 无 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从海水中提取金属镁的生产步骤有:①浓缩结晶脱水 ②加熟石灰 ③加盐酸 ④过滤 ⑤熔融电解,正确的生产顺序是
A.①②③④⑤ B.⑤④③①② C.②④③①⑤ D.③④②①⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.医用酒精是指质量分数为75%的乙醇溶液
B.用过滤的方法可以分离乙醇和乙酸乙酯
C.油脂、淀粉、纤维素、蛋白质都是高分子化合物
D.石油的裂解是使石油分馏产物中的长链烃断裂成乙烯、丙烯等气态短链烃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某地环保部门取一定量某工厂所排废水试样分成甲、乙、丙、丁四份,进行如图所示探究。

已知废水试样中可能含有下表中的离子:
阳离子 | Na+、Mg2+、X |
阴离子 | Cl-、SO、Y、NO |
(1)离子X是________(填化学式,下同),离子Y是________。
(2)表中不能确定是否存在的阴离子是________,能证明该阴离子是否存在的简单实验操作为______________________________________________
(3)丁组实验在酸性条件下发生反应的离子方程式是______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构简式如图所示,有关该有机物的叙述不正确的是( )
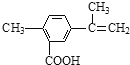
A.在一定条件下,能发生取代、氧化、酯化和加聚反应
B.该物质分子中最多可以有11个碳原子在同一平面上
C.1 mol该物质最多可与4 mol H2发生加成反应
D.1 mol该物质完全氧化最多可消耗14mol氧气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 元素周期律是元素原子核外电子排布周期性变化的结果
B. HF、HCl、HBr、HI的热稳定性和还原性从左到右依次减弱
C. 第三周期非金属元素含氧酸的酸性从左到右依次增强
D. 形成离子键的阴、阳离子间只存在静电吸引力
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com