
【题目】一定温度下,向2L恒容容器中充入1molA和1molB,发生反应A(g)+B(g)=C(g)经过一段时间后达到平衡,反应过程中测定的部分数据如表。下对说法正确的是( )
t/s | 0 | 5 | 15 | 25 | 35 | ||
n(A)/mol | 1.0 | 0.85 | 0.81 | 0.80 | 0.80 | ||
A. 前 5 s 的平均反应速率v(A)=0.03 mol·L-1·s-1
B. 正反应是吸热反应
C. 保持温度不变,起始时向容器中充入2molC,达平衡时,C的转化率大于80%
D. 保持温度不变,起始时向容器中充入0.2molA、0.2molB和1molC, 反应达到平衡前v(正)<v(逆)
【答案】D
【解析】
A.反应在前5 s的平均速率v(A)=![]() ,A错误;B.根据表中数据无法判断反应热,B错误;C.充入1.0mol A和1.0mol B,平衡时n(A)=n(B)=0.80mol,生成n(C)=△n(A)=0.20mol,则c(A)=c(B)=0.80mol÷2L=0.40mol/L,c(C)=0.20mol÷2L=0.10mol/L,化学平衡常数K=0.10/(0.40×0.40)=0.625;若起始时向容器中充入2.0 mol C,设剩余C的物质的量为xmol,则
,A错误;B.根据表中数据无法判断反应热,B错误;C.充入1.0mol A和1.0mol B,平衡时n(A)=n(B)=0.80mol,生成n(C)=△n(A)=0.20mol,则c(A)=c(B)=0.80mol÷2L=0.40mol/L,c(C)=0.20mol÷2L=0.10mol/L,化学平衡常数K=0.10/(0.40×0.40)=0.625;若起始时向容器中充入2.0 mol C,设剩余C的物质的量为xmol,则
A(g)+B(g)![]() C(g)
C(g)
开始(mol) 0 0 2.0
反应(mol)2.0-x 2.0-x 2.0-x
平衡(mol)2.0-x 2.0-x x
平衡时c(A)=c(B)=(2.0x)/2mol/L、c(C)=x/2mol/L,温度相同化学平衡常数相同,所以![]() =0.625,x=1.6,所以达到平衡时C的转化率是80%,C错误;D.相同温度下,起始时向容器中充入0.20 mol A、0.20 mol B和1.0 mol C,则浓度熵
=0.625,x=1.6,所以达到平衡时C的转化率是80%,C错误;D.相同温度下,起始时向容器中充入0.20 mol A、0.20 mol B和1.0 mol C,则浓度熵![]() >0.625,所以应达到平衡前v(正)<v(逆),D正确;答案选D。
>0.625,所以应达到平衡前v(正)<v(逆),D正确;答案选D。


科目:高中化学 来源: 题型:
【题目】氢能将成为21世纪的主要能源。太阳能光伏电池电解水可制高纯氢,工作示意图如下。通过控制开关连接K1或K2,可交替得到H2和O2。

(1)制H2时,连接________(填“K1”或“K2”),产生H2的电极反应式是____________,溶液pH___________(填“增大”、“减小”或“不变”)。
(2)改变开关连接方式,可得O2,此时电极3的反应式为:__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了检验淀粉水解的产物,设计如下实验方案:
![]()
请回答下列问题:
(1)试剂1为20%的H2SO4溶液,其作用是_________;
(2)试剂2为_________NaOH溶液,其作用是_________,使检验水解产物的实验得以顺利进行;发生反应的离子方程式为:_________;
(3)反应①的化学方程式为_________;
(4)为检验淀粉液是否已完全水解,取少量水解液于试管中,加入碘水,则证明淀粉未完全水解的现象是_________;
(5)如果实验过程中没有加入试剂2而直接加入试剂3,能否实现实验目的_________(填”能”或”否”)否,若不能,其原因是_________硫酸能溶解Cu(OH)2而使实验失败,最简单的改正措施是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知Ka(CH3COOH)=1.7×10-5,Kb(NH3·H2O)=1.7×10-5。25℃时,向40ml浓度均为0.01mol·L-1的盐酸和醋酸(1:1)混合溶液中逐滴加入0.10mol·L-1的氨水,测定过程中电导率和pH变化曲线如图所示,下列说法正确的是
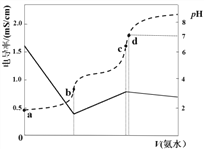
A. a点溶液中,c(CH3COO-)数量级约为10-5
B. b点溶液中,c(NH4+) < c(CH3COOH)
C. c点溶液中,c(NH4+) > c(Cl-)+c(CH3COO-)
D. d点水的电离程度大于c点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,在pH=5的CH3COOH溶液中存在如下电离平衡:CH3COOH![]() CH3COO-+H+,对于该平衡,下列叙述正确的是( )
CH3COO-+H+,对于该平衡,下列叙述正确的是( )
A.加入水时,平衡向右移动,CH3COOH电离常数增大
B.加入少量CH3COONa固体,平衡向右移动
C.加入少量NaOH固体,平衡向右移动,c(H+)减小
D.加入少量pH=5的硫酸,溶液中c(H+)增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,在一定体积pH=12的Ba(OH)2溶液中,逐滴加入一定物质的量浓度的NaHSO4溶液,当溶液中的Ba2+恰好完全沉淀时,溶液pH=11,若体积可以加和,则V (Ba(OH)2):V( NaHSO4)为( )
A.1:1B.1:4C.2:1D.3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A为羊肉的特征香味的成分,其合成路线如下:

![]()
已知:①RCH2CHO+HCHO![]()
![]() +H2O
+H2O
②![]()

![]()
③原醋酸三乙酯:![]()
(1)B是烃的含氧衍生物,质谱图表明B的相对分子质量为100,其中含氧元素的质量分数为16%。B能发生银镜反应,且分子结构中只有一个—CH3。B的结构简式为_______________________。
(2)D能发生的化学反应类型有________(填序号)。
①酯化反应 ②加成反应 ③消去反应 ④加聚反应
(3)下列关于E的说法中正确的是________(填序号)。
①E存在顺反异构 ②能使溴的四氯化碳溶液褪色
③能发生水解反应 ④分子式为C11H20O2
(4)写出B→C的化学方程式:____________________________________________________。
(5)写出酸性条件下F→A的化学方程式:__________________________________。
(6)若用系统命名法给A命名,A的名称为____________________________。
(7)与C含有相同官能团,分子结构中含有两个—CH3,一个![]() 的同分异构体有________种。
的同分异构体有________种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知CH4(g)+2O2(g)→CO2(g)+2H2O(g) ΔH== - Q1 ;
2H2(g)+O2(g) →2H2O(g) ΔH== - Q2;
H2O(g) →H2O(l) ΔH== - Q3
常温下,取体积比为4:1的甲烷和H2的混合气体112L(标准状况下),经完全燃烧后恢复到常温,则放出的热量为
A.4Q1+0.5Q2B.4Q1+Q2+10Q3C.4Q1+2Q2D.4Q1+0.5Q2+9Q3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列图所示所得出的结论正确的是
A.图甲是一定温度下,处于恒容密闭容器、弱酸性环境下的铁钉发生腐蚀过程中体系压强的变化曲线,可推知初始阶段铁钉主要发生析氢腐蚀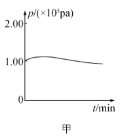
B.图乙是平衡体系2NO2(g)![]() N2O4(g);ΔH=-56.9 kJ·mol-1改变某一条件后v(正)、v(逆)的变化情况,可推知t0时刻改变的条件是升高温度
N2O4(g);ΔH=-56.9 kJ·mol-1改变某一条件后v(正)、v(逆)的变化情况,可推知t0时刻改变的条件是升高温度
C.图丙是某温度下c(CH3COOH)+c(CH3COO-)=0.100 mol·L-1的醋酸与醋酸钠混合溶液中c(CH3COOH)、c(CH3COO-)与pH的关系,可推知该温度下pH=3的溶液中:Ka<10-4.75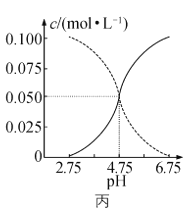
D.图丁中虚线是2SO2+O2![]() 2SO3在催化剂存在下反应过程中能量的变化情况,可推知催化剂Ⅰ的催化效果更好
2SO3在催化剂存在下反应过程中能量的变化情况,可推知催化剂Ⅰ的催化效果更好
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com