
| 10-4×10-4 |
| 0.1 |
| 10-4×10-4 |
| 0.1 |
| 10-14 |
| 10-4 |


科目:高中化学 来源: 题型:
| A、溶液中氢氧根离子的浓度增大了 |
| B、c(CH3COOH)减小,电离平衡向生成醋酸分子的方向移动? |
| C、平衡向电离的方向移动,氢离子的浓度增大,醋酸分子的数量减少 |
| D、电离程度增大,c(CH3COO-)也增大了 |
查看答案和解析>>
科目:高中化学 来源: 题型:
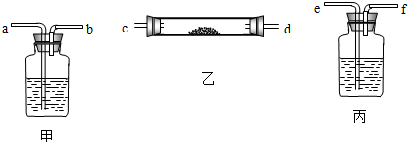
 如图是某学生设计的制取和收集某些气体的实验装置(可加热).
如图是某学生设计的制取和收集某些气体的实验装置(可加热).查看答案和解析>>
科目:高中化学 来源: 题型:
 A:在较高温度下和Br2按物质的量之比1:1发生加成反应的方程式:
A:在较高温度下和Br2按物质的量之比1:1发生加成反应的方程式:查看答案和解析>>
科目:高中化学 来源: 题型:
 在一定条件下,冰醋酸(纯净的醋酸)加水稀释过程中,溶液的导电能力(I)随加入水的体积(V)变化的曲线如图所示.
在一定条件下,冰醋酸(纯净的醋酸)加水稀释过程中,溶液的导电能力(I)随加入水的体积(V)变化的曲线如图所示.| c(H-) |
| c(CH3COOH) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com