
下列说法中不正确的是( )
A.常温下pH=7的溶液中:Fe3+、Mg2+、SO42-、Cl-能大量共存
B.在含有0.1mol·L-1 Fe3+的溶液中:SCN-、Cl-、K+不能大量共存
C.在含有HCO3-、SO32-、S2-、CH3COO-四种阴离子的溶液中加入足量的Na2O2固体后,
CH3COO-浓度变化最小
D.NaHSO4溶液与Ba(OH)2溶液反应至中性:2H++SO42-+Ba2++2OH- = BaSO4↓+2H2O
 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案科目:高中化学 来源:2016-2017学年云南省高二上期中化学试卷(解析版) 题型:选择题
用3块状大理石与30L3mol﹒L-1盐酸反应制取CO2气体,若要增大反应速率,可采取的措施是
①再加入30mL3 mol﹒L-1盐酸 ②改用30mL6 mol﹒L-1盐酸
③改用3g粉末状大理石 ④适当升高温度
A.①②④ B.②③④ C.①③④ D.①②③
查看答案和解析>>
科目:高中化学 来源:2017届云南省高三上第四次月考化学卷(解析版) 题型:选择题
将一定量的Mg和Cu组成的混合物加入到稀硝酸中,金属完全溶解(假设反应中还原产物只有NO)向反应后的溶液中加入3 mol/L NaOH溶液至沉淀完全,测得生成沉淀的质量比原来的混合物质量增加10.2 g。下列说法正确的是
A.当沉淀质量达到最大时,消耗NaOH溶液的体积一定大于200 mL
B.参加反应的金属的物质的量是0.3mol
C.将反应中生成的沉淀充分灼烧,得到固体的质量可能是10.8 g
D.金属完全溶解时收集到NO气体是0.1mol
查看答案和解析>>
科目:高中化学 来源:2017届山东省东营市高三上期中化学卷(解析版) 题型:选择题
已经部分被氧化的Fe-Cu合金样品(氧化产物为Fe2O3、CuO)共5.92g,经如下处理:

下列说法不正确的是
①滤液A中的阳离子为Fe2+、Fe3+、H+
②V=224mL ③V=336mL
④样品中含氧元素的物质的量为0.03mol
⑤溶解样品的过程中消耗硫酸的总物质的量为0.04mol
A.①③ B.①③④ C.②④⑤ D.③④⑤
查看答案和解析>>
科目:高中化学 来源:2017届山东省东营市高三上期中化学卷(解析版) 题型:选择题
(l) =H2O(g) △H1=a kJ·
=H2O(g) △H1=a kJ·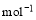
(2)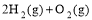 =2H2O(g) △H2=b kJ·
=2H2O(g) △H2=b kJ·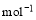
(3) =H2O(l) △H3=c kJ·
=H2O(l) △H3=c kJ·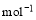
(4)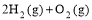 =2H2O(l) △H4=d kJ·
=2H2O(l) △H4=d kJ·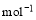
下列关系式中正确的是( )
A.a<c<0 B.b>d>0 C.2a=b<0 D.2c=d>0
查看答案和解析>>
科目:高中化学 来源:2017届山东省东营市高三上期中化学卷(解析版) 题型:选择题
下列物质中不能用化合反应的方法制得的是( )
①SiO2 ②H2SiO3 ③Fe(OH)3 ④CuS ⑤FeCl2 ⑥ CaSiO3
A.②④ B. ②④⑤ C.②③④⑤ D.②④⑥
查看答案和解析>>
科目:高中化学 来源:2017届宁夏高三上学期统练三化学试卷(解析版) 题型:填空题
CH4和H2O(g)可发生催化重整反应:CH4(g)+H2O(g) CO(g)+3H2(g)。
CO(g)+3H2(g)。
(1)已知:①2CO(g)+O2(g) 2CO2(g)△H1=akJ/mol
2CO2(g)△H1=akJ/mol
②CH4(g)+2O2(g) CO2(g)+2H2O(g)△H2=bkJ/mol
CO2(g)+2H2O(g)△H2=bkJ/mol
③CO(g)+H2O(g) CO2(g)+H2(g) △H3=ckJ/mol
CO2(g)+H2(g) △H3=ckJ/mol
④CH4(g)+H2O(g) CO(g)+3H2(g)△H4
CO(g)+3H2(g)△H4
由此计算△H4=________kJ/mol
(2)T℃时,向1L恒容密闭容器中投入1molCH4和1molH2O(g),发生反应:CH4(g)+H2O(g) CO(g)+3H2(g),经过tmin,反应达到平衡。已知平衡时.c(CH4)=0.5mol/L
CO(g)+3H2(g),经过tmin,反应达到平衡。已知平衡时.c(CH4)=0.5mol/L
①0~tmin内,该反应的平均反应速率v(H2)=____________。
②T℃时,该反应的平衡常数K=___________。
③当温度升高到(T+l00)℃时,容器中c(CO)=0.75mol/L,则该反应是___________反应(填“吸热”或“放热”)。
(3)工业上用CO与H2在催化剂作用下合成CH3OH,其反应为:CO(g)+2H2(g) CH3OH(g)。按n(CO):n(H2)=1:2向密闭容器中充入反应物,测得平衡时混合物中CH3OH的体积分数在不同压强下随温度的变化如图所示。
CH3OH(g)。按n(CO):n(H2)=1:2向密闭容器中充入反应物,测得平衡时混合物中CH3OH的体积分数在不同压强下随温度的变化如图所示。

①P1__________P2(填“<”“>”或“=”)
②在C点时,CO转化率为____________。
查看答案和解析>>
科目:高中化学 来源:2017届宁夏高三上学期统练三化学试卷(解析版) 题型:选择题
科学家开发出一种新型锂-氧电池,其能世密度极高,效率达到90%以上,电池中添加碘化锂(LiI)和微量水。工作原理如图所示,总反应为:O2+4LiI+2H2Og 2I2+4LiOH。对于该电池的下列说法不正确的是
2I2+4LiOH。对于该电池的下列说法不正确的是
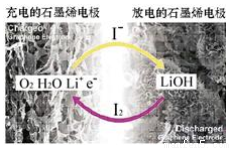
A.充电时阴极反应为LiOH+e-=Li+OH-
B.充电时Li+从阳极区移向阴极区
C.放电时正极反应为O2+2H2O+4Li++4e-=4LiOH
D.放电时负极上I-被氧化
查看答案和解析>>
科目:高中化学 来源:2016-2017年吉林长春白城一中两校高二上期中化学卷(解析版) 题型:选择题
质 量分数为46%的乙醇水溶液中,水分子和乙醇分
量分数为46%的乙醇水溶液中,水分子和乙醇分 子中氢原子个数比为
子中氢原子个数比为
A.2:1 B.1:1 C.1:2 D.1:3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com