
| m |
| V |
| 0.0153��0.005 |
| 0.005��0.015 |
| ||
| 0.02mol |
| 0.2L |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
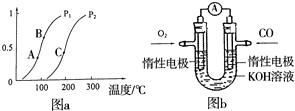
| A�����Է����еķ�Ӧһ����Ѹ�ٷ�����Ӧ |
| B�����Է����еķ�Ӧһ�������ܷ�����Ӧ |
| C�����Է����еķ�Ӧʵ�ʿ���û�з�����Ӧ |
D�������£�2H2O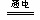 2 H2����O2������������ˮ�ķֽⷴӦ���Է���Ӧ 2 H2����O2������������ˮ�ķֽⷴӦ���Է���Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��+172.51kJ/mol | B��-283.01kJ/mol |
| C��+283.01kJ/mol | D��+504.00kJ/mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ��ʴ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����101kPaʱ��1mol������ȫȼ��ʱ���ų������������������ʵ�ȼ���� |
| B����ͼ���кͷ�Ӧ����1molˮ����ʱ�ķ�Ӧ�Ƚ��к��� |
| C��ȼ���Ȼ��к����Ƿ�Ӧ�ȵ�����֮һ |
| D�����ȷ�Ӧû�����ü�ֵ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
A��C2H6(g) ��  O2(g)��2CO2(g) ��3H2O(l)��H =��1560kJ��mol��1 O2(g)��2CO2(g) ��3H2O(l)��H =��1560kJ��mol��1 |
| B��2C2H6(g) �� 7O2(g)��4CO2(g) ��6H2O(g)��H =��1560kJ��mol��1 |
| C��2C2H6(g) �� 7O2(g)��4CO2(g) ��6H2O(l)��H =��3120 kJ��mol��1 |
D��C2H6(g) �� O2(g)��2CO2(g) ��3H2O(l)��H =��52.0kJ��mol��1 O2(g)��2CO2(g) ��3H2O(l)��H =��52.0kJ��mol��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��c(H+)=c(OH-)=10-6mol/L��Һ | B��pH=7����Һ |
| C��ʹʯ����Һ����ɫ����Һ | D�������ǡ����ȫ��Ӧ�������ε���Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
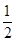 O2��g���TCO��g����H1����110��5kJ/mol
O2��g���TCO��g����H1����110��5kJ/mol| A����̼��ȼ�����á�H3��ʾ�����H3����H1 |
| B����̼��ȼ�����á�H3����ʾ�����H3����H1 |
| C��Ũ������ϡNaOH��Һ��Ӧ���к���ֵΪ57��3kJ��mol-1 |
| D��ϡ������ϡNaOH��Һ��Ӧ����1molˮ���ų�57��3kJ������ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com