
【题目】探索二氧化碳在海洋中转移和归宿,是当今海洋科学研究的前沿领域。研究表明,溶于海水的二氧化碳主要以无机碳形式存在,其中HCO3-占95%。科学家利用下图所示装置从海水中提取CO2,有利于减少环境温室气体含量。

下列说法不正确的是
A. a室中OH-在电极板上被氧化
B. b室发生反应的离子方程式为:H+ + HCO3- = CO2↑ + H2O
C. 电路中每有0.2mol 电子通过时,就有0.2mol阳离子从c室移至b室
D. 若用氢氧燃料电池供电,则电池负极可能发生的反应为:H2 + 2OH- - 2e- =2H2O
科目:高中化学 来源: 题型:
【题目】如图是A分子的球棍模型和B分子的比例模型,回答下列问题:

(1)A和B的关系是 。
(2)写出A分子在催化剂存在条件下加热和氧气反应的化学方程式 。
(3)写出B分子和金属钠反应的化学方程式 。
(4)B在加热条件下能够和HBr发生反应生成溴乙烷,该反应类型是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①2K2CrO4+H2SO4![]() K2Cr2O7+K2SO4+H2O ②K2Cr2O7+6FeSO4+7H2SO4
K2Cr2O7+K2SO4+H2O ②K2Cr2O7+6FeSO4+7H2SO4![]() 3Fe2(SO4)3+ Cr2(SO4)3 +K2SO4+7H2O ③Fe2(SO4)3+2HI
3Fe2(SO4)3+ Cr2(SO4)3 +K2SO4+7H2O ③Fe2(SO4)3+2HI![]() 2FeSO4+I2+H2SO4下列结论正确的是( )
2FeSO4+I2+H2SO4下列结论正确的是( )
A.①②③均是氧化还原反应
B.反应③中生成0.1 mol I2时转移电子数为0.1 NA
C.反应②中氧化剂与还原剂的物质的量之比为6:1
D.氧化性强弱顺序是K2Cr2O7>Fe2(SO4)3>I2
查看答案和解析>>
科目:高中化学 来源: 题型:
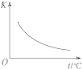
【题目】工业上制备H2的一种重要方法是:CO(g)+H2O(g) ![]() CO2(g)+H2(g) ΔH=Q kJ·mol―1。已知该反应的平衡常数K与温度的关系如图所示。若在一固定的密闭容器中,850 ℃时发生上述反应,并测得容器内各物质的浓度(mol·L―1)随时间的变化关系如下表:
CO2(g)+H2(g) ΔH=Q kJ·mol―1。已知该反应的平衡常数K与温度的关系如图所示。若在一固定的密闭容器中,850 ℃时发生上述反应,并测得容器内各物质的浓度(mol·L―1)随时间的变化关系如下表:
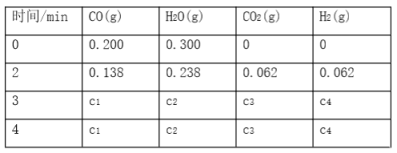
已知:850 ℃时该反应的化学平衡常数K=1.0,请回答下列问题:
(1)下列可以判断该反应达到化学平衡状态的是________。
A.单位时间内减少CO(g)的浓度等于生成CO2(g)的浓度
B.反应容器内的压强不发生变化
C.混合气体中H2(g)的浓度不再发生改变
D.氢气的生成速率等于水的消耗速率
(2)Q______0(填“>”“=”或“<”)。
(3)若在850 ℃时向反应容器中充入H2O(g),K值________________(填“增大”“减小”或“不变”)。
(4)上表中c2为________________,CO(g)的转化率为________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物H是一种有机光电材料中间体。实验室由芳香化合物A制备H的一种合成路线如下:
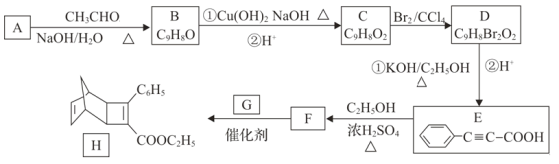
已知:①RCHO+CH3CHO![]()
![]()
![]() RCH=CHCHO
RCH=CHCHO
②![]()
③ +HCHO
+HCHO![]()
 +HCOO-
+HCOO-
回答下列问题:
(1)E中含氧官能团名称为_________非含氧官能团的电子式为_______。E的化学名称为苯丙炔酸,则B的化学名称为__________。
(2)C→D的反应类型为__________。B→C的过程中反应①的化学方程式为 ________。
(3)G的结构简式为_________。
(4)写出同时满足下列条件的F的一种同分异构体的结构简式________。
①遇FeCl3溶液显紫色;②能发生银镜反应;③分子中有五种不同化学环境的氢且个数比为1:1:2:2:4
(5)写出用甲醛和乙醇为原材料制备化合物C(CH2ONO2)4的合成路线(其他无机试剂任选,合成路线流程图示例见本题题干)。_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新能源汽车的核心部件是锂离子电池,常用磷酸亚铁锂(LiFePO4)做电极材料。对LiFePO4废旧电极(含杂质Al、石墨粉)回收并获得高纯Li2CO3的工业流程图如下:

资料:碳酸锂在水中溶解度:
温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
溶解度/g | 1.54 | 1.33 | 1.17 | 1.01 | 0.85 | 0.72 |
(1)过程i研磨粉碎的目的是_______。
(2)过程ii加入足量NaOH溶液的作用是______。
(3)过程iii采用不同氧化剂分别进行实验,均采用Li含量为3.7%的原料,控制pH为3.5,浸取1.5h后,实验结果如下表所示:
序号 | 酸 | 氧化剂 | 浸出液Li+浓度(g/L) | 滤渣中Li含量/% |
实验1 | HCl | H2O2 | 9.02 | 0.10 |
实验2 | HCl | NaClO3 | 9.05 | 0.08 |
实验3 | HCl | O2 | 7.05 | 0.93 |
①实验2中,NaClO3与盐酸反应生成黄绿色气体,大大增加了酸和氧化剂的用量,该反应的离子方程式为______。
②结合实验结果和①中的现象,最终选择H2O2作为氧化剂,原因是______。
③过程iii得到的浸出液循环两次的目的是_____。
(4)浸出液中存在大量H2PO4和HPO42,已知:H2PO4 HPO42 +H+,HPO42 PO43+H+,结合平衡移动原理,解释过程iv得到磷酸铁晶体的原因_____。
(5)对比过程iv和v,说明过程iv不用饱和Na2CO3溶液的原因______。
(6)简述过程vi的操作_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂用软锰矿(主要成分是MnO2,含少量Al2O3和SiO2)和闪锌矿(主要成分是ZnS,含少量FeS、CuS等杂质)为原料制备MnO2和Zn(干电池原料),其简化流程如下:

已知:反应Ⅰ中所有金属元素均以离子形式存在。回答下列问题:
(1)滤渣1中除了SiO2以外,还有一种淡黄色物质,该物质是由MnO2、CuS与硫酸共热时产生的,请写出该反应还原产物的化学式____。
(2)反应Ⅱ中加入适量金属锌的目的是为了回收某种金属,请写出该反应的离子方程式______。
(3)反应Ⅲ中X可以是______。(填字母代号)它的作用是______。
a.MgO b.Zn(OH)2 c.Cu2(OH)2CO3 d.MnCO3
(4)反应Ⅳ中电极均是惰性电极,写出阴极电极反应式_______________。
(5)已知:H2S的电离常数K1=1.0×107,K2=7.0×1015。0.1 mol/L NaHS的pH__7(填“>”“=”或“<”),理由是____。
(6)在废水处理领域中常用H2S将Mn2+转化为MnS除去,向含有0.020 mol·L1 Mn2+废水中通入一定量的H2S气体,调节溶液的pH=a,当HS浓度为1.0×104 mol·L1时,Mn2+开始沉淀,则a=_____。[已知:Ksp(MnS)=1.4×1015]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高纯六水氯化锶晶体(SrCl2·6H2O)可作有机合成的催化剂。用碳酸锶矿石(含少量BaCO3、FeO、SiO2等杂质)制备高纯六水氯化锶晶体的过程如图所示。
已知:

I.25℃,Ksp[Fe(OH)3]=1.0×10-38 ,Ksp[Fe(OH)2]=1.0×10-16
Ⅱ.SrCl2·6H2O晶体在61℃时开始失去结晶水,100℃时失去全部结晶水。
请回答:
(1)步骤①中将矿石制成浆液能加快反应速率的原因是_____________________________。
(2)在“浆液”中加入工业盐酸,测得锶的浸出率与温度、时间的关系如图所示:

据此合适的工业生产条件为_________________________。
(3)步骤②“溶液”中加入30%的H2O2,其作用是_____________________________(用离子方程式表示)。
(4)步骤③所得滤渣的主要成分除Fe(OH)3外,还有_______________________(填化学式);25℃,为使Fe3+沉淀完全需调节溶液pH值最小为_____________(当离子浓度减小至1.0×10-5mol·L-1时,可认为沉淀完全)。
(5)关于上述流程中各步骤的说法,正确的是___________(填标号)。
A.步骤④用60℃的热水浴加热蒸发至有晶膜出现
B.步骤④冷却结晶过程中应通入HC1气体
C.步骤⑤干燥SrCl2·6H2O晶体可以采用减压干燥
(6)为测定所得SrCl2·6H2O(Mr=267)晶体样品的纯度,设计了如下方案:称取1.10g样品溶解于适量水中,向其中加入含AgNO31.70g的AgNO3溶液(溶液中除Cl-外,不含其它与Ag+反应生成沉淀的离子),C1-即被全部沉淀。然后用含Fe3+的溶液作指示剂,用0.100 mol·L-1的NH4SCN标准溶液滴定剩余的AgNO3溶液,使剩余的Ag+以AgSCN白色沉淀的形式析出,当___________时达到滴定终点,用去NH4SCN溶液20.00 mL,则原SrCl2·6H2O晶体的纯度为________________%(计算结果保留1位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最新研究表明As2O3在医药领域有重要应用。某小组从工业废料中提取As2O3设计流程如下:

已知:H3AsO3为弱酸,热稳定性差。
(1)写出一条“碱浸”时提高浸取率的方法____;“碱浸”中H3AsO3转化成Na3AsO3的离子方程式为____。
(2)“氧化”时常在向混合液中通入O2时对体系加压,目的是____。
(3)“沉砷”过程中有如下反应:
①![]()
![]() <0
<0
②![]()
![]() >0
>0
沉砷率与温度关系如图。沉砷最佳温度为____,高于85℃时,沉砷率下降的原因是____。

(4)“还原”过程中获得H3 AsO3的化学反应方程式为____;“操作A”为:____、过滤;滤液Ⅱ的主要成分是____。
(5)若每步均完全反应,“氧化’’和“还原”时消耗相同条件下O2和SO2体积分别为xL、yL,则废水中n(H3AsO3):n(H3AsO4)=____(写出含x、y的计算式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com