
硫酸钙是一种用途非常广泛的产品,可用于生产硫酸、漂白粉等一系列物质(见图).下列说法正确的是()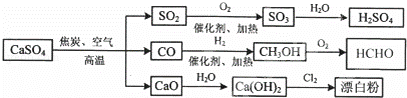
A. CO、SO2、SO3均是酸性氧化物
B. 除去与水反应,图示转化反应均为氧化还原反应
C. 工业上利用Cl2和澄清石灰水反应来制取漂白粉
D. 用CO合成CH3OH进而合成HCHO的两步反应,原子利用率均为100%
考点: 含硫物质的性质及综合应用;氯气的化学性质.
专题: 氧族元素.
分析: A.酸性氧化物是一类能与水作用生成酸或与碱作用生成盐和水或与碱性氧化物反应生成盐的氧化物;
B.凡是有化合价升降的反应都是氧化还原反应;
C.工业上常用氯气和消石灰反应来制取漂白粉;
D.原子利用率是指反应物中的所有原子进入期望产物中的百分比.
解答: 解:A.CO不能与碱反应,不是酸性氧化物,故A错误;
B.除去与水反应,图示转化反应都是与氧气反应或氢气反应,都一定有化合价升降,均为氧化还原反应,故B正确;
C.澄清石灰水中氢氧化钙的浓度较小,应用纯净的消石灰,故C错误;
D.工业上一般采用下列两种反应合成甲醇:
反应Ⅰ:CO(g)+2H2(g) 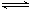 CH3OH(g)△H1
CH3OH(g)△H1
反应Ⅱ:CO2(g)+3H2(g) 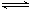 CH3OH(g)+H2O(g)△H2
CH3OH(g)+H2O(g)△H2
反应Ⅱ中不是所有原子进入期望产物,原子利用率不为100%,故D错误.
故选B.
点评: 本题考查酸性氧化物、氧化还原反应、漂白粉的制取、原子利用率,难度不大,注意澄清石灰水中氢氧化钙的浓度较小,应用纯净的消石灰制取漂白粉.


科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的数值,下列说法正确的是()
A. 1mol某烷烃分子中含8 mol氢原子,则1 mol该烷烃分子中共价键数为8NA
B. 标准状况下,a L氧气和氮气的混合物中含有的分子数为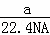
C. 1.4g乙烯分子中含有0.05NA个C=C键
D. 1mol Cl2发生反应时,转移的电子数一定是2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
以下有关物质的质量分数和物质的量浓度的叙述正确的是()
A. 等体积硫酸铁、硫酸铜、硫酸钾溶液分别与足量的氯化钡溶液反应,若生成硫酸钡沉淀的质量相等,则三种硫酸盐溶液的物质的量浓度之比为1:1:1
B. Na2O2和Na2O各0.1mol分别放入100g水中,所得溶液的物质的量浓度不相等
C. 质量分数分别为5%和15%的氨水等体积混合后所得溶液的质量分数为10%
D. 20℃时,饱和KCl溶液的密度为1.174g•cm﹣3,物质的量浓度为4.0 mol•L﹣1,则此溶液中KCl的质量分数为 ×100%
×100%
查看答案和解析>>
科目:高中化学 来源: 题型:
把500mLNH4HCO3和Na2CO3的混合溶液分成五等份,取一份加入含a mol氢氧化钠的溶液恰好反应完全,另取一份加入含b mol HCl的盐酸恰好反应完全,则该混合溶液中c(Na+)为()
A. 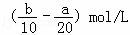 B. (2b﹣a)mol/L C.
B. (2b﹣a)mol/L C. 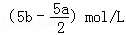 D. (10b﹣5a)mol/L
D. (10b﹣5a)mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
下列表示对应化学反应的离子方程式正确的是( )
A. MnO2 与浓盐酸反应制Cl2:MnO2+4HCl Mn2++2Cl﹣+Cl2↑+2H2O
Mn2++2Cl﹣+Cl2↑+2H2O
B. 明矾溶于水产生Al(OH)3胶体:Al3++3H2O═Al(OH)3↓+3H+
C. Na2O2溶于水产生O2:Na2O2+H2O═2Na++2OH﹣+O2↑
D. Ca(HCO3)2溶液与少量NaOH溶液反应:HCO3﹣+Ca2++OH﹣═CaCO3↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A.离子晶体中可能含有共价键,但不一定含有金属元素
B.分子晶体中一定含有共价键
C.非极性分子中一定存在非极性键
D.对于组成和结构相似的分子晶体,一定是相对分子质量越大,熔、沸点越高
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com