
常温下,将0.01 mol的NH4Cl和0.002 mol NaOH溶于水配成溶液。
(1)该溶液中存在的平衡体: ;
; 。
(2)溶液中共有 种不同的粒子。
(3)这些粒子中浓度为0.01 mol·L-1的是 ,浓度为0.002 mol·L-1是 。
(4)物质的量之和是0.01 mol的三种微粒是: 。
科目:高中化学 来源:2015-2016学年广东省高二上学期期中考试化学试卷(解析版) 题型:填空题
减少污染、保护环境是全世界最热门的课题。请回答下列问题:
(1)为减少SO2的排放,常采取的措施有:
①将煤转化为清洁气体燃料。已知:H2(g)+1/2O2(g)=H2O(g) 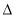 H= -241.8KJ/mol
H= -241.8KJ/mol
C(s)+1/2O2(g)=CO(g) 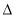 H= -110.5KJ/mol
H= -110.5KJ/mol
写出焦炭与水蒸气反应的热化学方程式 ;
②洗涤含SO2的烟气,以下物质可作洗涤剂的是 ;
a.Ca(OH)2 b.Na2CO3 c.CaCl2 d.NaHSO3、
(2)污染物CO在催化剂作用下可以与H2反应生成甲醇:CO(g)+2H2(g)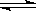 CH3OH(g)。
CH3OH(g)。
①在恒容体系中,可以判断反应达到平衡状态的依据是 (填序号).
a. v正(CH3OH)= v逆(CO) b. 混合气体的密度不变
c. 混合气体的平均相对分子质量不变 d. c(CO):c(H2): c( CH3OH)= 1:2:1
②在密闭容器中充有10molCO与20molH2,CO的平衡转化率与温度、压强的关系如下图
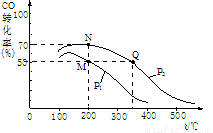
M、N、Q三点的平衡常数KM、KN、KQ的大小关系为____ __。
(3)汽车尾气中NOx和CO的生成及转化为:
① 已知气缸中生成NO的反应为:N2(g)+O2(g) 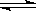 2NO(g)
2NO(g) 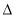 H>0
H>0
汽车启动后,气缸温度越高,单位时间内NO排放量越大,原因是 。
② 若加入1mol空气(含有0.8molN2和0.2molO2),1300℃时在密闭容器内反应达到平衡,测得NO为8×10-4mol。计算该温度下的平衡常数K(写出计算过程,计算过程中数据可作近似处理)
③ 汽车燃油不完全燃烧时产生CO,有人设想按下列反应除去CO:
2CO(g)=2C(s)+O2(g) 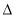 H>0,该设想能否实现? (选填“能”或“不能”),依据是 。
H>0,该设想能否实现? (选填“能”或“不能”),依据是 。
④ 目前,在汽车尾气系统中装置催化转化器可减少CO和NO的污染,其化学反应方程式为 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河南省高二上学期期中考试化学试卷(解析版) 题型:选择题
市场上经常见到的标记为Li-ion的电池称为“锂离子电池”。它的负极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导Li的高分子材料。这种锂离子电池的电池反应为: Li+2Li0.35NiO2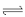 2Li0.85NiO2 ,下列说法不正确的是( )
2Li0.85NiO2 ,下列说法不正确的是( )
A.放电时,负极的电极反应式:Li-e-=Li+
B.充电时,Li0.85NiO2既发生氧化反应又发生还原反应
C.该电池不能用水溶液作为电解质
D.放电过程中Li+向负极移动
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河南省高一上学期期中考试化学试卷(解析版) 题型:选择题
向FeCl3溶液中加入过量的Cu,反应结束后,溶液中大量存在的金属离子是
A.Fe2+、Cu2+ B.Fe3+、Fe2+ C.Cu+、Cu2+ D.Cu2+、Fe3+
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河南省高一上学期期中考试化学试卷(解析版) 题型:选择题
将2mol·L-1盐酸10mL稀释到200mL,再取出1mL,这1mL溶液的物质的量浓度是
A.0.05mol·L-1 B.0.25mol·L-1 C.0.1mol·L-1 D.0.5mol·L-1
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河南省高二上学期期中考试化学试卷(解析版) 题型:选择题
在蒸发皿中加热蒸干下列物质的溶液并灼烧,可得原有物质的固体是( )
A. 氯化铝 B.碳酸氢镁 C.硫酸亚铁 D.碳酸钠
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高一上学期第二次月考化学试卷(解析版) 题型:填空题
现有含NaCl、Na2SO4和NaNO3的混合物,选择适当的试剂将其转化为相应的沉淀或固体,从而实现Cl-、SO42-、和NO3-的相互分离。相应的实验过程可用下图表示:请回答下列问题

(1)写出实验流程中下列物质的化学式:试剂X ,沉淀A 。
(2)按此实验方案得到的溶液3中肯定含有 (填化学式)杂质;为了解决这个问题,可以向溶液3中加入适量的 。
(3)上述实验流程中加入过量的Na2CO3的目的是____________,确认Na2CO3已过量的实验方法是:___________________________
(4)写出步骤①中发生反应的离子方程式:__________________________________;
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省、高安二中高二上期中联考化学试卷(解析版) 题型:选择题
根据碘与氢气反应的热化学方程式:
①I2(g)+H2(g)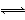 2HI(g) ΔH=-9.48 kJ·mol-1
2HI(g) ΔH=-9.48 kJ·mol-1
②I2(s)+H2(g)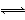 2HI(g) ΔH=+26.48 kJ·mol-1
2HI(g) ΔH=+26.48 kJ·mol-1
下列判断中正确的是( )
A.254 g I2(g)中通入2 g H2(g),反应放热9.48 kJ
B.1 mol固态碘与1 mol气态碘所含的能量相差17.00 kJ
C.反应①的产物比反应②的产物稳定
D.物质的量相同时,反应②的反应物总能量比反应①的反应物总能量低
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东省高一上学期期中考试化学试卷(解析版) 题型:选择题
下列应用或事实与胶体的性质没有关系的是( )
A.在江河入海处易形成三角洲
B.用石膏或盐卤点制豆腐
C.在FeCl3溶液中滴加NaOH溶液出现红褐色沉淀
D.清晨的阳光穿过茂密的林木枝叶所产生的美丽的光线
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com