
【题目】孟鲁司特钠可用于抗新型冠状病毒肺炎,其制备中间体G 的一种合成路线如下:
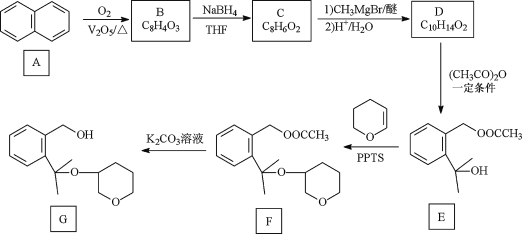
已知:① B、C除苯环外还含有一个五元环,D的苯环上只有两个取代基;
②RX![]() RMgX
RMgX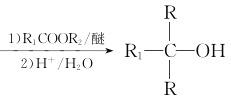
回答下列问题:
(1)A 的化学名称是____________________。
(2)F中含氧官能团名称是____________________________。
(3)B的结构简式为 ______________________________________。
(4)D生成E同时生成乙酸的化学方程式为___________________________________。
(5)E生成F的反应类型是________________。
(6)化合物 W 与G 互为同分异构体,能发生水解反应,其核磁共振氢谱有四组峰且峰面积之比为9:9:2:2,则 W 的结构简式为_____________________(写一种) 。
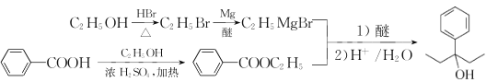
(7)设计以苯甲酸和乙醇为起始原料制备3-苯基-3-戊醇(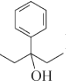 )的合成路线: _____________________________________________(无机试剂及有机溶剂任用) 。
)的合成路线: _____________________________________________(无机试剂及有机溶剂任用) 。
【答案】萘 醚键、酯基 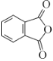
 +(CH3CO)2O
+(CH3CO)2O![]()
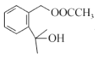 + CH3COOH 加成反应
+ CH3COOH 加成反应 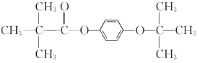 或
或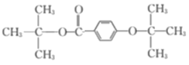
【解析】
A为![]() ,由B的分子式结合信息①,可确定B的结构简式为
,由B的分子式结合信息①,可确定B的结构简式为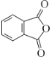 ;由C的分子式,结合信息①,参照E的结构,可确定C的结构简式为
;由C的分子式,结合信息①,参照E的结构,可确定C的结构简式为![]() ;由D的分子式结合E的结构,可确定D结构简式为
;由D的分子式结合E的结构,可确定D结构简式为![]() ;E与
;E与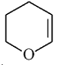 发生加成反应生成F;F在碱性条件下水解生成G。据此解答。
发生加成反应生成F;F在碱性条件下水解生成G。据此解答。
(1)A 为![]() ,化学名称是萘。答案为:萘;
,化学名称是萘。答案为:萘;
(2)F的结构简式为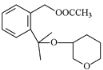 ,含氧官能团名称是醚键、酯基。答案为:醚键、酯基;
,含氧官能团名称是醚键、酯基。答案为:醚键、酯基;
(3)由以上分析,可得出B的结构简式为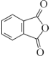 。答案为:
。答案为: ;
;
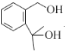
(4) 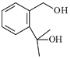 生成
生成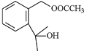 同时生成乙酸的化学方程式为
同时生成乙酸的化学方程式为![]() +(CH3CO)2O
+(CH3CO)2O![]()
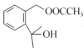 + CH3COOH。答案为:
+ CH3COOH。答案为: +(CH3CO)2O
+(CH3CO)2O![]()
 + CH3COOH;
+ CH3COOH;
(5) 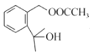 与
与 反应生成
反应生成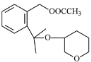 的反应类型是加成反应。答案为:加成反应;
的反应类型是加成反应。答案为:加成反应;
(6)化合物 W 与G 互为同分异构体,能发生水解反应,则含有酯基,即含有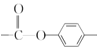 或
或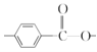 结构片断,核磁共振氢谱有四组峰且峰面积之比为9:9:2:2,则苯环上的两个取代基应在对位,且存在两组
结构片断,核磁共振氢谱有四组峰且峰面积之比为9:9:2:2,则苯环上的两个取代基应在对位,且存在两组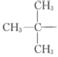 ,则同分异构体的结构简式为
,则同分异构体的结构简式为 或
或 。答案为:
。答案为: 或
或 ;
;
(7)从信息看,应将苯甲酸转化为苯甲酸酯,然后与CH3CH2MgBr发生反应,而CH3CH2MgBr又需将乙醇转化为CH3CH2Br,进而转化为CH3CH2MgBr。合成路线: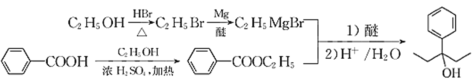 。答案为:
。答案为: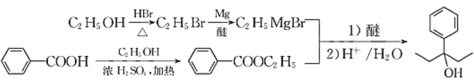 。
。


科目:高中化学 来源: 题型:
【题目】某中学化学课外兴趣小组通过实验探究Fe2+、Fe3+的性质。回答下列问题:
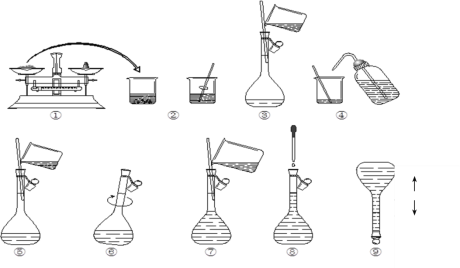
(1)本次实验中共需要1mol/LFeCl2溶液100 mL,配制时涉及到如下操作:
①步骤③中玻璃棒的作用是__;
②在配制溶液过程中步骤⑦所进行的操作是___(填“洗涤”、“转移”、“定容”);该步中视线应与溶液凹液面的最低处保持___。
③下列操作会使所配溶液物质的量浓度偏低的是___。
A.溶解后小烧杯、玻璃棒没有洗涤
B.所用容量瓶中,已有少量蒸馏水
C.定容、加盖倒转摇匀后,发现液面低于刻度线,又滴加蒸馏水至刻度线
(2)取2mLFeCl2溶液于试管中,加入几滴氯水,再加入1滴KSCN溶液,观察到的现象为__,说明Cl2可将Fe2+氧化成Fe3+。FeCl2溶液与氯水反应的离子方程式为___,此时将所取FeCl2溶液完全反应需__molCl2。
(3)在(2)溶液中加入过量的铁粉,溶液变成___色;发生反应的离子方程式为__,此时溶液中所含铁元素的微粒的物质的量为__mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘海醇是一种临床中应用广泛的非离子型造影剂,具有耐受性好,毒性低等优点,利用碘海醇做造影剂进行肺部CT检查,能为新冠肺炎确诊及治疗提供重要参考,碘海醇的一种合成路线如下:
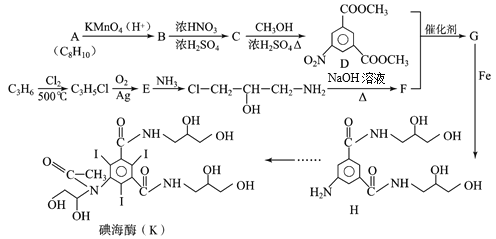
已知:①![]()
②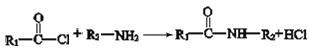
(1)已知A是苯的同系物,则A的结构简式为________。
(2)C中所含官能团的名称为_________。
(3)写出C→D的化学反应方程式_________。
(4)E的结构简式为_______。
(5)M与B互为同分异构体,M是含有苯环的酯类物质,能发生银镜反应,且苯环上一氯取代物有两种。写出任意一种符合上述条件的M的结构简式________。
(6)上述合成路线中,由合成碘海醇过程如下,下列说法正确的是________。
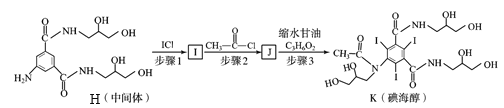
a. 步骤1中1 mol H需消耗3 mol ICl,并且有副产物HCl生成
b. 步骤2和步骤3中的反应类型相同
c. 碘海醇极易溶于水与其结构中存在较多的羟基有关
(7)有机物Q(C3H8O3)可由油脂水解制得,已知合成路线中的物质B可与Q形成交联聚合物P,P的结构片段如下:
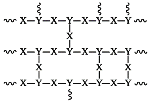
①其中![]() 的结构简式为_______。
的结构简式为_______。
②写出一定条件下相同物质的量的B与Q反应,形成线型高分子的化学方程式_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以含镍废硫酸盐(含 Ni2+ 、Fe2+ 、Cu2+ 、Co2+ 、A13+ 、Mn2+ 、Cr3+ 、Mg2+ 、Zn2+ 等)为原料制取NiSO4·6H2O 的工艺流程如下:
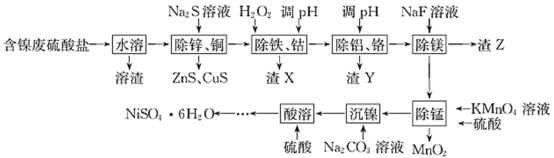
相关金属离子形成氢氧化物沉淀的pH 范围如下:
金属离子 | Co2+ | Co3+ | Fe2+ | Fe3+ | A13+ | Cr3+ | Ni2+ |
开始沉淀的pH | 7.2 | 0.23 | 6.3 | 1.5 | 4.1 | 4.3 | 6.9 |
沉淀完全的pH | 9.2 | 1.1 | 8.3 | 2.8 | 5.4 | 5.6 | 8.9 |
回答下列问题:
(1)已知1gKsp(CuS)= -47.6,1gKsp(ZnS)= -23.8,则反应ZnS+Cu2+![]() CuS+Zn2+的平衡常数对数值1gK= ________________________。
CuS+Zn2+的平衡常数对数值1gK= ________________________。
(2)“除铁、钴”时,加入H2O2的目的是 ______________,得到的渣X为________。
(3) “除铝、铬”时,调pH 范围为 _________;滤渣Y 中含Cr(OH)3,其性质与 A1(OH)3 类似,写出Cr(OH)3与NaOH反应的化学方程式: __________________。
(4)“除锰”时,发生反应的离子方程式为___________________________。
(5)“酸溶”得到溶液制备 NiSO4·6H2O晶体,还需进行的操作工艺是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图所示装置,当X、Y选用不同材料时,可将电解原理广泛应用于工业生产。下列说法中正确的是
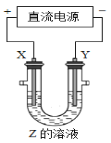
A. 氯碱工业中,X、Y均为石墨,Y附近能得到氢氧化钠
B. 铜的精炼中,X是纯铜,Y是粗铜,Z是CuSO4
C. 电镀工业中,X是待镀金属,Y是镀层金属
D. 外加电流的阴极保护法中,X是待保护金属
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是由常见元素组成的一些单质及其化合物之间的转化关系图。各方框表示有关的一种反应物或生成物(部分物质已经略去)。其中A、B、D在常温下均为无色无味的气体,C是能使湿润的红色石蕊试纸变蓝的气体,M是最常见的无色液体。

(1)写出C→E的化学方程式: 。
(2)实验室常用加热两种固体混合物的方法制备物质C,其化学方程式为: ,干燥C常用 (填写试剂名称)。
(3)E物质遇到D物质时,会观察到 现象,若用排水法收集F,则最终集气瓶中收集到的气体为 (填写物质的化学式)。
(4)写出A→D的化学方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W有如图所示的转化关系,则X、Y可能是
①C,CO ②AlCl3、Al(OH)3 ③Na、Na2O ④NaOH、Na2CO3 ⑤AlO2-,Al(OH)3 ⑥Fe FeCl2
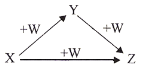
A.①②⑥B.①②③④⑤C.①②③④⑤⑥D.①②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二甲醚和乙醇是两种常见的有机溶剂,也可作为新能源。
(1)通过以下反应可获得二甲醚(CH3OCH3):
①CO(g)+H2O(g)=CO2(g)+H2(g) ΔH 1=a kJ·molˉ1
②CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH 2=b kJ·molˉ1
③2CH3OH(g)=CH3OCH3(g)+H2O(g) ΔH 3=c kJ·molˉ1
则反应 2CO(g)+4H2(g)=CH3OCH3(g)+H2O(g)的 ΔH=_________kJ·molˉ1。
(2)已知气相直接水合法可以制取乙醇:H2O(g)+C2H4(g) ![]() CH3CH2OH(g)。
CH3CH2OH(g)。
在 n(H2O)∶n(C2H4)=1∶1 的条件下投料,乙烯的平衡转化率与温度(T)及压强(p) 的关系如图1所示。
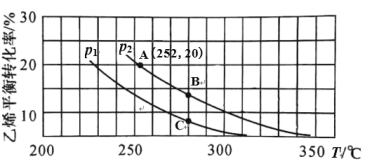 图1
图1
①下列有关说法中正确的是_________。
A.p1>p2 B.280℃时,vB>vC
C.A、B、C 三点的平衡常数 KA>KB>KC D.低温有利于该反应自发进行
②在 p2,280℃条件下,C 点的 v 正 ____v 逆 (填“>”、“<”或“=”),理由是________。
③计算图 1 中 A 点的平衡常数 Kp=_________。(结果用 p2 的代数式表示,平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
(3)在 n(H2O)∶n(C2H4)=1∶x 的条件下投料,某研究小组在压强为 p2,温度为 252℃ 时,进行平衡体系中乙醇的体积分数随投料比变化的测定实验。在图 2 中画出平衡体系中乙醇的体积分数 φ 随 x 变化的示意图____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,相同pH的盐酸和醋酸分别加水稀释至平衡,pH随溶液体积变化的曲线如下图所 示。据图判断正确的是
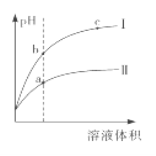
A. Ⅱ为盐酸稀释时的pH变化曲线
B. b点溶液的导电性比c点溶液的导电性强
C. a点KW的数值比c点KW的数值大
D. b点酸的总浓度大于a点酸的总浓度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com