
常温下,在一定体积pH=12的Ba(OH)2溶液中,逐滴加入一定物质的量浓度的NaHSO4溶液,当溶液中的Ba2+恰好完全沉淀时,溶液pH=11。若反应后溶液的体积等于Ba(OH)2溶液与NaHSO4溶液的体积之和,则Ba(OH)2溶液与NaHSO4溶液的体积比是
A.1∶9 B.1∶1 C.1∶2 D.1∶4
 春雨教育同步作文系列答案
春雨教育同步作文系列答案科目:高中化学 来源: 题型:
密闭容器中发生下列反应aA(g)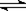 cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是
cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是
A.A的转化率变小 B.平衡向正反应方向移动
C.D的体积分数变大 D.a > c+d
查看答案和解析>>
科目:高中化学 来源: 题型:
合成氨反应的平衡状态是指下列情况中的
A.氢气的消耗速率与氨生成的速率之比为3︰2
B.体积不变时,混合气体的密度不再改变
C.氮气的生成速率与氨的生成速率之比为1︰2
D.容器内物质的总质量不变
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,甲、乙两杯醋酸稀溶液,甲的pH=a,乙的pH=a+1,对下列叙述的判断正确的是
A.甲中水电离出来的H+的物质的量浓度是乙中水电离出来的H+的物质的量浓度的10倍
B.物质的量浓度c(甲)>10c(乙)
C.中和等物质的量的NaOH溶液需甲、乙两杯醋酸溶液的体积,V(甲)=10V(乙)
D.甲中的c(OH-)为乙中的c(OH-)的10倍
查看答案和解析>>
科目:高中化学 来源: 题型:
恒温下,将amol N2与bmol H2的混合气体通入一个固定容积的密闭容器中,发生如下反应:N2(g)+3H2(g)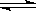 2NH3(g)
2NH3(g)
⑴若反应进行到某时刻t时,nt(N2)=13mol,nt(NH3)=6mol,则a= 。
⑵反应达平衡时,混合气体的体积为716.8L(标准状况下),其中NH3的含量(体积分数)为25%。平衡时NH3的物质的量 。
⑶原混合气体中,a∶b= 。
⑷达到平衡时,N2和H2的转化率之比,α(N2)∶α(H2)=
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下,可逆反应X(g)+3Y(g)  2Z(g),若X、Y、Z起始浓度分别为c1、c2、c3(均不为0),平衡时,X、Y、Z的浓度分别为0.1 mol/L,0.3 mol/L,0.08 mol/L,则下列判断不合理的是
2Z(g),若X、Y、Z起始浓度分别为c1、c2、c3(均不为0),平衡时,X、Y、Z的浓度分别为0.1 mol/L,0.3 mol/L,0.08 mol/L,则下列判断不合理的是
A.c1:c2= 1:3 B.X、Y的转化率相等
C.平衡时,Y和Z的生成速率之比为2:3
D.c1的取值范围为0<c1﹤0.14 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
下表为元素周期表的—部分,请参照元素①一⑨在表中的位置,回答下列问题。
| 族
| IA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(1)第三周期中元素非金属性最强的元素的原子结构示意图是___________。
(2)②③⑦最高价氧化物对应水化物酸性由强到弱的顺序是___________(填化学式)。
(3)用电子式表示③的氢化物:_________________________________。
(4)下列可以判断⑤和⑥金属性强弱的是______________________(填序号)。
a. 单质的熔点⑤比⑥低 b. 化合价⑤比⑥低
c. 单质与水反应⑤比⑥剧烈 d. 最高价氧化物的水化物的碱性⑤比⑥强
(5)含有上述元素的物质间存在以下转化:
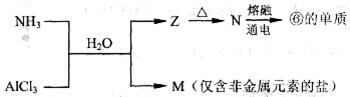
a. Z的化学式是___________。
b. N生成⑥的单质反应的化学方程式是_________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com