
【题目】下列有关说法正确的是( )
A.金属钠、镁着火时可用泡沫灭火器扑灭
B.为防止试管破裂,加热固体时试管口一般要略高于试管底
C.1L pH=13的Ba(OH)2溶液中含有0.2NA个OH﹣ 离子
D.1.2克CH4所含有的共价键数与0.1 mol NH3所含的共价键数相同
【答案】D
【解析】解:A.钠燃烧生成过氧化钠,过氧化钠、镁都与二氧化碳反应,不能用二氧化碳灭火,应用沙土盖灭,故A错误;B.加热固体时,应防止生成的水冷凝时导致试管炸裂,加热固体时试管口一般要略低于试管底,故B错误;
C.pH=13的Ba(OH)2溶液中c(OH﹣ )=0.1mol/L,1LpH=13的Ba(OH)2溶液中含有0.1NA个OH﹣ 离子,故C错误;
D.n(CH4)= ![]() =0.075mol,则CH4所含有的共价键为0.075mol×4=0.3mol,与0.1 mol NH3所含的共价键数相同,故D正确.
=0.075mol,则CH4所含有的共价键为0.075mol×4=0.3mol,与0.1 mol NH3所含的共价键数相同,故D正确.
故选D.
【考点精析】认真审题,首先需要了解钠的化学性质(钠的化学性质:与非金属反应;与水反应;与酸反应;与盐溶液反应).


 孟建平名校考卷系列答案
孟建平名校考卷系列答案科目:高中化学 来源: 题型:
【题目】已知氢化锂(LiH)属于离子晶体,LiH跟水反应可以放出氢气。下列叙述中正确的是( )
A.LiH的水溶液显中性
B.LiH中氢离子半径比锂离子半径大
C.LiH中氢离子可以被还原成氢气
D.反应生成的氧化产物和还原产物的质量比为:12:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由下列实验及现象不能推出相应结论的是( )
实验 | 现象 | 结论 | |
A. | 向2 mL 0.1 | 黄色逐渐消失,加KSCN溶液颜色不变 | 还原性: |
B. | 将金属钠在燃烧匙中点燃,迅速伸入集满CO2的集气瓶 | 集气瓶中产生大量白烟,瓶内有黑色颗粒产生 | CO2具有氧化性 |
C. | 加热盛有少量NH4HCO3固体的试管,并在试管口放置湿润的红色石蕊试纸 | 石蕊试纸变蓝 | NH4HCO3显碱性 |
D. | 向2支盛有2 mL相同浓度银氨溶液的试管中分别加入2滴相同浓度的NaCl和Nal溶液 | 一只试管中产生黄色沉淀,另一支中无明显现象 |
|
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列试剂中,能够鉴别BaCl2 、NaCl 、Na2CO3的最佳试剂是( )
A. 稀盐酸 B. NaOH溶液 C. 稀硫酸 D. AgNO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应是吸热反应的是( )
A.C+CO2 ![]() 2CO
2CO
B.Fe+H2SO4═FeSO4+H2↑
C.2Al+Fe2O3 ![]() 2Fe+Al2O3
2Fe+Al2O3
D.2Na2O2+2H2O═4NaOH+O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在两份相同的Ba(OH)2溶液中,分别滴入物质的量浓度相等的H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示.下列分析不正确的是( ) 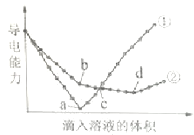
A.①代表滴加H2SO4溶液的变化曲线
B.b点,溶液中大量存在的离子是Na+、OH﹣
C.c点,两溶液中含有相同量的OH﹣
D.a、d两点对应的溶液均显中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于弱酸,在一定温度下达到电离平衡时,各微粒的浓度存在一种定量的关系.下表为几种弱酸在25℃时的电离平衡常数
酸 | 电离平衡常数K |
CH3COOH | 1.76×10﹣5 |
H2CO3 | K1=4.3×10﹣7 K2=5.61×10﹣11 |
H3PO4 | K1=7.52×10﹣3 K2=6.23×10﹣8 K3=2.20×10﹣13 |
回答下列问题:
(1)从电离的角度,HCO ![]() 、HPO
、HPO ![]() 、H2PO4﹣都可看作是酸,其中酸性最强的是 , 最弱的是 .
、H2PO4﹣都可看作是酸,其中酸性最强的是 , 最弱的是 .
(2)电离平衡常数是用实验的方法测定出来的.现已经测得25℃时,c mol/L的CH3COOH的电离转化率为a,则该温度下醋酸的电离平衡常数KCH3COOH= .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据题意解答
(1)某温度下,Kw=10﹣12 . 若保持温度不变,向少量水中加入g的NaOH固体,并加水稀释至1L,才能使溶液中水电离产生的H+、OH﹣的浓度乘积即:c(H+)水c(OH﹣)水=10﹣26 . 若保持温度不变,向水中通入的HCl气体恰好使溶液中c(H+)/c(OH﹣)=1010 , 则此时水电离的c(OH﹣)=molL﹣1 .
(2)一定温度下,现有a.盐酸,b.硫酸,c.醋酸 三种酸
①当三种酸体积相同,物质的量浓度相同时,使其恰好完全中和所需NaOH的物质的量由大到小的顺序是 . (用a、b、c表示)
②当三者c(H+)相同且体积也相同时,分别放入足量的锌,相同状况下产生气体的体积由大到小的顺序是 . (用a、b、c表示)
③当c(H+)相同、体积相同时,同时加入形状、密度、质量完全相同的锌,若产生相同体积的H2(相同状况),则开始时反应速率的大小关系为 . (用a、b、c表示)
(3)现有两瓶pH=2的盐酸和醋酸溶液,简述如何用最简单的方法区别盐酸和醋酸.(限选试剂:石蕊试液、酚酞试液、pH试纸、蒸馏水).采用的方法为 .
(4)执信中学A学生为了测定某烧碱样品的纯度,准确称量8.2g含有少量中性易溶杂质的样品,配成500mL待测溶液.用0.200 0molL﹣1的标准盐酸进行滴定,选择甲基橙作指示剂,试根据实验回答下列问题:
①滴定过程中,眼睛应注视;滴定终点时,溶液从色变为色, .
②观察酸式滴定管液面时,开始俯视,滴定终点平视,则滴定结果(填“偏高”、“偏低”或“无影响”);若将锥形瓶用待测液润洗,然后再加入10.00mL待测液,则滴定结果(填“偏高”、“偏低”或“无影响”).
③根据如表数据,通过标准酸滴定,计算待测烧碱溶液的物质的量浓度是 , 烧碱样品的纯度是 . (本小题计算结果保留4位有效数字)
滴定次数 | 待测溶液 | 标准酸体积 | |
滴定前的刻度(mL) | 滴定后的 | ||
第①次 | 10.00 | 0.40 | 20.50 |
第②次 | 10.00 | 4.10 | 24.00 |
第③次 | 10.00 | 2.20 | 23.80 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com