
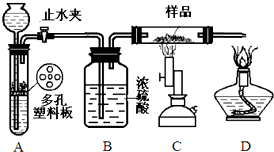
分析 根据图象知,A装置实验目的是制取还原性气体,用的是简易启普发生器制取气体,可以用稀硫酸和Zn制取氢气;B装置作用是干燥气体,C装置用氢气还原红色物质,用酒精灯点燃未反应的氢气;
(1)利用压强差检验装置气密性;
(2)打开止水夹生成氢气,通过后续装置充满氢气排出装置中的空气后,检验气体纯度,收集检验氢气纯度,气体纯净后点燃C处的酒精喷灯,反应完成熄灭C处的酒精喷灯,待C处冷却至室温后,关闭止水夹,防止生成的铜被空气中氧气氧化;
(3)A、Fe2O3与硫酸反应生成硫酸铁,也可以是氧化铜和氧化亚铜的混合物,若固体是Fe2O3和Cu2O的混合物,放入足量稀硫酸中会有Cu生成,Cu恰好能将Fe3+还原为Fe2+,固体全部溶解;
B、固体若是Fe2O3和Cu2O的混合物,放入足量稀硫酸中会有Cu生成,Cu能将Fe3+还原为Fe2+,剩余固体可以是铜;
C、若固体全部溶解,所得溶液中滴加 KSCN 试剂时溶液不变红色,则一定是Fe2O3和Cu2O的混合物,放入足量稀硫酸中发生反应生成硫酸铁、硫酸铜、铜,有Cu生成,固体恰好完全溶解,向溶液中滴加KSCN,溶液不变红色,则生成Cu能与Fe3+恰好完全反应Fe2+;
另取少量样品于试管中,加入适量的浓硝酸,产生红棕色的气体,氧化亚铜的氧化性大于硫离子,证明样品中一定含有Cu2O,氧化亚铜和浓硝酸反应生成硝酸铜,二氧化氮和水;
(4)2Fe3++Cu=Cu2++2Fe2+,Cu2O+2H+═Cu+Cu2++H2O,固体为铜,铁离子全部反应生成亚铁离子,结合化学方程式定量关系计算得到.
解答 解:根据图象知,A装置实验目的是制取还原性气体,用的是简易启普发生器制取气体,可以用稀硫酸和Zn制取氢气;B装置作用是干燥气体,C装置用氢气还原红色物质,用酒精灯点燃未反应的氢气;
(1)利用压强差检验装置气密性,其检验方法为:向装置A中的长颈漏斗内注入液体至形成一段液注,若液柱高度保持不变,则该装置气密性良好,
故答案为:向装置A中的长颈漏斗内注入液体至形成一段液注,若液柱高度保持不变;
(2)氢气混有空气加热发生爆炸,所以开始先通氢气,打开止水夹生成氢气,通过后续装置充满氢气,目的是排出装置中的空气,检验最后U型管出来的气体氢气纯度,气体纯净后再点燃C处的酒精喷灯,反应完成后先撤酒精灯,玻璃管冷却再停氢气,操作位熄灭C处的酒精喷灯,待C处冷却至室温后,关闭止水夹,防止生成的铜被空气中氧气氧化,所以其排列顺序是①⑤④②③;
故答案为:①⑤④②③;
(3)A、固体全部溶解,若固体是Fe2O3和Cu2O的混合物,放入足量稀硫酸中会有Cu生成,Cu恰好能将Fe3+还原为Fe2+,故A错误;
B、固体若是Fe2O3和Cu2O的混合物,放入足量稀硫酸中会有Cu生成,Cu能将Fe3+还原为Fe2+,剩余铜,故B错误;
C、若固体全部溶解,再滴加KSCN溶液,溶液不变红色,因为Cu2O溶于硫酸生成Cu和CuSO4,而H2SO4不能溶解Cu,所以混合物中必须有Fe2O3存在,使其生成的Fe3+溶解产生的Cu,反应的有关离子方程式为Fe2O3+6H+=2Fe3++3H2O、Cu2O+2H+=Cu+Cu2++H2O、2Fe3++Cu=2Fe2++Cu2+.说明样品一定含有Fe2O3和Cu2O,故C正确;
另取少量样品于试管中,加入适量的浓硝酸,产生红棕色的气体,氧化亚铜的氧化性大于硫离子,证明样品中一定含有Cu2O,氧化亚铜和浓硝酸反应生成硝酸铜,二氧化氮和水,反应的化学方程式为:Cu2O+6HNO3(浓)=2Cu(NO3)2+2NO2↑+3H2O,
故答案为:C;Cu2O;Cu2O+6HNO3(浓)=2Cu(NO3)2+2NO2↑+3H2O;
(4)2Fe3++Cu=Cu2++2Fe2+,Cu2O+2H+═Cu+Cu2++H2O,固体为铜,铁离子全部反应生成亚铁离子,生成1.0molFe2+,消耗Cu0.5mol,剩余Cu物质的量=$\frac{3.2g}{64g/mol}$=0.05mol,原样品中Cu2O物质的量=0.05mol+0.5mol=0.55mol,
故答案为:0.55.
点评 本题考查了物质组成的分析判断,实验过程分析应用,主要是氧化还原反应发生的条件,产物判断,掌握基础是关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
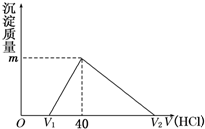 将一定量的钠铝合金置于水中,合金全部溶解,得到20mL pH=14的溶液,然后用1mol/L的盐酸滴定,沉淀质量与消耗盐酸的体积关系如下图所示,则下列选项正确的是( )
将一定量的钠铝合金置于水中,合金全部溶解,得到20mL pH=14的溶液,然后用1mol/L的盐酸滴定,沉淀质量与消耗盐酸的体积关系如下图所示,则下列选项正确的是( )| A. | 图中m值为1.56 g | B. | 标准状况下产生氢气896 mL | ||
| C. | 图中V2为60 mL | D. | 原合金质量为0.92 g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁制自来水管不能与铜制水龙头连接 | |
| B. | 红热的铁丝与水接触,表面形成蓝黑色的保护层 | |
| C. | 白铁表面有划损时,也能阻止铁被腐蚀 | |
| D. | 家用炒菜铁锅用水清洗放置后,出现红棕色的锈渍 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 Ⅰ.写出下列化学方程式:
Ⅰ.写出下列化学方程式:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 23 g Na与足量H2O反应完全后可生成NA个H2分子 | |
| B. | 1 mol Na2O2和足量CO2反应转移2 NA个电子 | |
| C. | 标准状况下,22.4 L N2和H2混合气中含NA个原子 | |
| D. | 3 mol单质Fe完全转变为Fe3O4,失去8 NA个电子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com