
| ̽������ | ʵ�鷽�� | ʵ������ | д���������ӷ���ʽ |
| ̽��Fe2+���л�ԭ�� | ȡ����0.1mol��L-1FeCl2��Һ����������KSCN��Һ��������Һ�м������� | ��Һ�Ȳ���죬 ���ΪѪ��ɫ | ��Fe2+�����ķ�Ӧ�� |
| ̽��Fe3+���������� | ȡ����0.1mol��L-1FeCl3��Һ���������� ��������Һ�м�������KSCN��Һ | ��Һ����ΪѪ��ɫ | ��Fe3+�����ķ�Ӧ�� |
| ̽������ | ʵ�鷽�� | ʵ������ | д���������ӷ���ʽ |
| ̽��Fe2+���л�ԭ�� | ������Һ�м������� ������ˮ | ��Һ�Ȳ���죬�� ��ΪѪ��ɫ ��ΪѪ��ɫ | �� Fe2+�����ķ�Ӧ�� 2Fe2++Cl2=2Fe3++ 2Cl- |
| ̽��Fe3+���������� | �������� ���� | ��Һ����ΪѪ��ɫ | ��Fe3+�����ķ�Ӧ�� 2 Fe3++ Fe= 3Fe2+ |


 ǧ�������������ĩ�����Ծ�����ϵ�д�
ǧ�������������ĩ�����Ծ�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��������ˮ�������c��H+����pH =5��CH3COOH��Һ��pH =5������ |
| B�����뾶��Fe(OH)3������K+��C1-��Na+ |
| C�����µ����ʵ���Ũ����Һ��pH��Na2CO3�������ƣ�NaHCO3 |
| D���⻯��ķе㣺H2Se��H2S��H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��CO2+H2O==H2CO3 | B��H2CO3==CO2��+H2O |
| C��CaCO3+2HCl==CaCl2+H2O+CO2�� | D��CO2+C����2CO |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��2CO + O2 = 2CO2 | B��2Fe2O3 + 3CO =" 4Fe" + 3CO2 |
| C��C + CO2 = 2CO | D��C + H2O =" CO" + H2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������1.60g | B������1.60g����2.50g |
| C������2.50g | D������2.50g |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
A��Na+�Ľṹʾ��ͼ�� 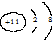 | B��ˮ���ӵĵ���ʽ��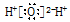 |
| C��������̼�Ľṹʽ��O=C=O | D��̼�����Ƶĵ��뷽��ʽ��NaHCO3= Na+ + HCO3�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��N2O��H2O | B��N2��O2��H2O | C��N2��HNO3��H2O | D��NH3��NO��H2 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com