
下列实验误差分析错误的是( )
A. 用润湿的pH试纸测稀碱溶液的pH,测定值偏小
B. 用容量瓶配制溶液,定容时俯视刻度线,所配溶液浓度偏小
C. 滴定前滴定管内无气泡,终点读数时有气泡,所测体积偏小
D. 测定中和反应的反应热时,将碱缓慢倒入酸中,所测温度值偏小
 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源:2016-2017学年山东省高二下学期开学考试化学试卷(解析版) 题型:选择题
为探究金属的腐蚀情况,某同学将锌片和铜片置于浸有饱和食盐水和酚酞的滤纸上,并构成如图所示的装置。下列判断合理的是( )
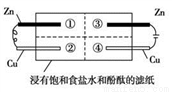
A. 左边铜片上有气泡冒出 B. 右边锌片上的反应为2Cl-- 2e-= Cl2↑
C. 最先观察到红色的区域是② D. 两铜片质量均不发生变化
查看答案和解析>>
科目:高中化学 来源:2017届辽宁省庄河市高三上学期期末考试理综化学试卷(解析版) 题型:选择题
乙二酸(HOOC—COOH)与丁醇(C4H10O)反应,形成的二酯最多有(不含立体异构)
A. 6种 B. 8种 C. 10种 D. 12种
查看答案和解析>>
科目:高中化学 来源:2016-2017学年甘肃省天水市高二下学期开学考试(寒假作业检测)化学试卷(解析版) 题型:填空题
下图所示装置中,甲、乙、丙三个烧杯依次分别盛放100 g 5.00%的NaOH溶液、足量的CuSO4溶液和100 g 10.00%的K2SO4溶液,电极均为石墨电极。
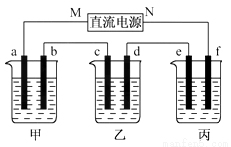
(1)接通电源,经过一段时间后,测得丙中K2SO4浓度为10.47%,乙中c电极质量增加。据此回答问题:
①电源的N端为____________极;
②电极b上发生的电极反应为____________________;
③列式计算电极b上生成的气体在标准状况下的体积:________________;
④电极c的质量变化是__________g;
⑤电解前后各溶液的酸、碱性大小是否发生变化,简述其原因:
甲溶液__________________;乙溶液___________________;丙溶液______________;
(2)如果电解过程中铜全部析出,此时电解能否继续进行,为什么? _____________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年甘肃省天水市高二下学期开学考试(寒假作业检测)化学试卷(解析版) 题型:选择题
一定温度下,在2 L的密闭容器中发生如下反应:A(s)+2B(g)  xC(g) △H<0,B、C的物质的量随时间变化的关系如图1,达平衡后在t1、t2、t3、t4时都只改变了一种条件,逆反应速率随时间变化的关系如图2
xC(g) △H<0,B、C的物质的量随时间变化的关系如图1,达平衡后在t1、t2、t3、t4时都只改变了一种条件,逆反应速率随时间变化的关系如图2
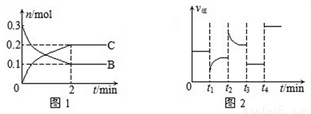
下列有关说法正确的是
A. x=2,反应开始2 min内,v(A)=0.05 mol/(L·min)
B. t1时改变的条件是降温,平衡逆向移动
C. t2时改变的条件可能是增大C的浓度,t2时正反应速率减小
D. t3时可能是减小压强,平衡不移动;t4时可能是使用催化剂,c(B)不变
查看答案和解析>>
科目:高中化学 来源:2016-2017学年甘肃省天水市高二下学期开学考试(寒假作业检测)化学试卷(解析版) 题型:选择题
下列说法错误的有
①化学反应除了生成新物质外,还伴随着能量的变化
②放热反应不需要加热就能发生
③需要加热才能发生的反应都是吸热反应
④化学反应放热还是吸热。决定于生成物具有的总能量和反应物具有的总能量的大小
⑤热化学方程式应注明反应时的温度与压强,如没注明则表示常温常压时的反应
⑥等量的氢气和氧气分别完全燃烧生成气态水和液态水,前者放出的热量多
⑦H2(g)+I2(g)  2HI(g) ΔH=-QkJ·mol-1表示常温常压下,在恒温密闭容器中当有1mol H2和1mol I2(g)反应生成2 mol HI时放出QkJ的热量
2HI(g) ΔH=-QkJ·mol-1表示常温常压下,在恒温密闭容器中当有1mol H2和1mol I2(g)反应生成2 mol HI时放出QkJ的热量
⑧同温同压下,H2(g)+Cl2(g)===2HCl(g)在光照条件下和点燃条件下的ΔH相同
A. 2项 B. 3项 C. 4项 D. 5项
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省景德镇市高二(素质班)上学期期末考试化学试卷(解析版) 题型:选择题
下列各项内容中排列顺序正确的是
A. 相同物质的量浓度的下列溶液中NH4+的浓度: (NH4)2SO4> NH4Cl > NH4HCO3
B. 微粒半径: K+> S2-> F-
C. 给出质子的能力:CH3COOH >C2H5OH > H2O
D. 氢化物的沸点: HF > HCl > HBr
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省庄河市高一上学期期末考试化学试卷(解析版) 题型:实验题
实验室拟用浓盐酸与二氧化锰反应制取纯净的氯气。并验证氯气的性质。
(Ⅰ)制取氯气:
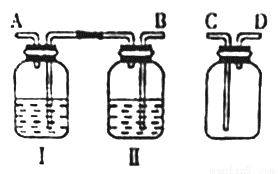
(1)按气体从左到右流动的方向将下列装置进行连接(填字母〉,H→_____、_______→ _______。广口瓶Ⅱ中的试剂为________。
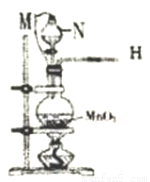
(2)仪器N的名称是_______;M是连通上下玻璃仪器的橡胶管,其目的是__________________;写出圆底烧瓶中发生反应的离子方程式_________________。
(3)连接好仪器后,上述装置存在一个明显的缺陷,你的改进方法是_______________。
(Ⅱ)验证氯气的性质:将从上述发生装置H处导出的气体依次经过下列装置验证氯气的性质(其他相关装置已略去)
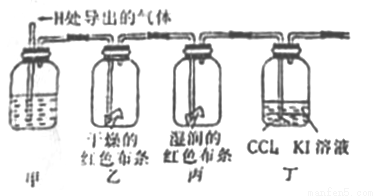
(4)丁中出现的现象是__________________,该反应证明了氯气的____________性。
(5)证明HClO具有漂白性的实验现象是__________________,甲中的试剂是_________。
查看答案和解析>>
科目:高中化学 来源:2017届山东省淄博市高三第一次模拟考试化学试卷(解析版) 题型:选择题
可逆反应L(s )+aG(g)?bR(g)△H 达到平衡时、温度和压强对该反应的影响如图所示:x轴表示温度,y轴表示平衡混合气中G的体积分数,压强pl>p2。下列判断正确的是
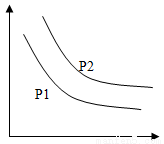
A. 1+a<b B. △H<0 C. a>b D. 增加L的物质的量,可提高G的转化率
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com