
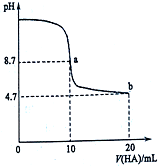
 室温下向10mL 0.1mol•L-1NaOH溶液中加入0.1mol•L-1的一元酸HA溶液pH的变化曲线如图所示.下列说法不正确的是( )
室温下向10mL 0.1mol•L-1NaOH溶液中加入0.1mol•L-1的一元酸HA溶液pH的变化曲线如图所示.下列说法不正确的是( )| A. | 在逐滴加入HA溶液至20mL时,NaOH溶液中水的电离程度先增大后减小 | |
| B. | b点所示溶液中c(A-)>c(HA) | |
| C. | pH=7时,c(Na+)=c(A-)+c(HA) | |
| D. | 该酸是弱酸 |
分析 A.氢氧化钠溶液中加入酸HA,开始碱性减弱,水的电离程度增大,加入10mLHA时恰好反应,而后HA过量,在20mL时溶液呈酸性,抑制水的电离;
B.a点时酸碱恰好中和,溶液pH=8.7,说明HA为弱酸,b点为等浓度NaA、HA混合溶液,溶液呈酸性,说明HA的电离程度大于A-的水解程度;
C.pH=7时,溶液中c(H+)=c(OH-),结合电荷守恒判断;
D.a点时酸碱恰好中和,溶液pH=8.7,说明HA为弱酸,NaA溶液水解呈碱性.
解答 解:A.氢氧化钠溶液中加入酸HA,开始碱性减弱,水的电离程度增大,加入10mLHA时恰好反应,而后HA过量,在20mL时溶液呈酸性,抑制水的电离,在逐滴加入HA溶液至20mL时,NaOH溶液中水的电离程度先增大后减小,故A正确;
B.a点时酸碱恰好中和,溶液pH=8.7,说明HA为弱酸,b点为等浓度NaA、HA混合溶液,溶液呈酸性,说明HA的电离程度大于A-的水解程度,则:c(A-)>c(HA),故B正确;
C.pH=7时,溶液中c(H+)=c(OH-),由电荷守恒可知c(Na+)+c(H+)=c(A-)+c(OH-),则c(Na+)=c(A-),故C错误;
D.a点时酸碱恰好中和,溶液pH=8.7,说明HA为弱酸,故D正确.
故选:C.
点评 本题考查酸碱混合的定性判断及溶液pH的计算,题目难度中等,明确各点对应溶质组成为解答关键,注意掌握电荷守恒、物料守恒及盐的水解原理在判断离子浓度大小中的应用,试题培养了学生的灵活应用能力.


 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案科目:高中化学 来源: 题型:填空题

 .
. .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 实验室要配制2mol/L稀硫酸250mL.
实验室要配制2mol/L稀硫酸250mL.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
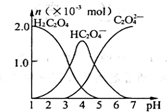 常温下,向10mL 0.2mol•L-1草酸(H2C2O4)溶液中逐滴加入等浓度的NaOH溶液.有关微粒的物质的量与混合溶液的pH有如图关系,下列说法正确的是
常温下,向10mL 0.2mol•L-1草酸(H2C2O4)溶液中逐滴加入等浓度的NaOH溶液.有关微粒的物质的量与混合溶液的pH有如图关系,下列说法正确的是| A. | HC2O4-在溶液中水解程度大于电离程度 | |
| B. | 当V(NaOH)=10 mL,时,溶液中水的电离程度比纯水大 | |
| C. | 当V(NaOH)=15 mL,时,溶液中存在:c(Na+)>c(HC2O4-)>c(C2O42-)>c(OH-)>c(H+) | |
| D. | 当V(NaOH)=20 mL,时,溶液中存在:c(OH-)=c(HC2O4-)+2c(H2C2O4)+c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c (K+)>c (CH3COO-)>c(H+)>c (OH-) | B. | c(K+)=c (CH3COO-)>c (OH-)=c (H+) | ||
| C. | c(K+)+c (H+)═c(CH3COOH)+c (OH-) | D. | c (CH3COOH)+c (CH3COO-)=0.01mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 编号 | 盐酸 | 氢氧化钠 | △t/℃ |
| 1 | 0.1mol•L-1 | 0.05mol•L-1 | 3.5 |
| 2 | 0.1mol•L-1 | 0.1mol•L-1 | x |
| 3 | 0.2mol•L-1 | 0.2mol•L-1 | 14 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸铜与烧碱溶液反应:CuSO4+2OH-═Cu(OH)2↓+SO42- | |
| B. | 钠与水反应:Na+2H2O═Na++2OH-+H2↑ | |
| C. | 碳酸钠溶液中加入足量盐酸:Na2CO3+2H+═Na++CO2↑+H2O | |
| D. | 氢氧化铝中和胃酸(盐酸):Al(OH)3+3H+═Al3++3H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 35.7g | B. | 30g | C. | 17g | D. | 9g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com