
【题目】已知反应:X(g)+2Y(g)![]() 3Z(g) △H=-akJ·mol-1(a>0)。下列说法正确的是
3Z(g) △H=-akJ·mol-1(a>0)。下列说法正确的是
A. 达到平衡状态时,放出的热量一定小于a kJ
B. 向体系中加入X(g)时,正、逆反应速率一定都增大
C. 当容器内的压强保持不变时,则反应一定达到平衡状态
D. 若Y与Z的物质的量之比保持不变,则反应达到平衡状态
 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案科目:高中化学 来源: 题型:
【题目】在密闭容器中发生反应2SO2(g)+O2(g) 2SO3(g) △H<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,针对图像下列分析正确的是
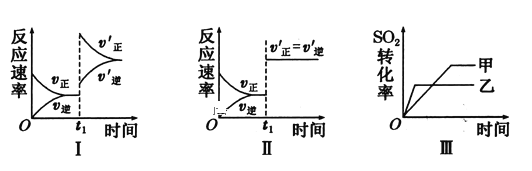
A.图I研究的是t1时刻升高温度对反应速率的影响
B.图I研究的是加入合适催化剂对反应速率的影响
C.图II研究的是t1时刻通入氦气(保持恒容)对反应速率的影响
D.图III研究的是温度对化学平衡的影响,且乙的温度较高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上以钛铁矿(主要成分为钛酸亚铁(FeTiO3),含有MgO、SiO2等杂质)为原料,制备金属钛和铁红的工艺流程如下:

已知:酸溶时,FeTiO3转化为Fe2+和TiO2+
(1)FeTiO3中Ti元素的化合价为_____价,铁红的用途为____________(任写一种)。
(2) “水解”中,发生反应的离子方程式为______________________________。
(3) “沉铁”中,生成的酸性气态产物的电子式为______________;该过程控制反应温度低于35℃,原因为_______________________________________。
(4)FeCO3转化为铁红时,发生的化学方程式为_______________________________。
(5)制得的FeCO3可加入足量的稀硫酸,则从溶液中获得绿矾的操作是_____________。
(6)电解生产钛时用TiO2 和石墨做电极,电解质为熔融的CaO,则阴极的反应式为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了探究Cu(NO3)2 的氧化性和热稳定性,某化学兴趣小组设计了如下实验。
Ⅰ.Cu(NO3)2 的氧化性
将光亮的铁丝伸入Cu(NO3)2 溶液中,一段时间后将铁丝取出。为检验溶液中Fe 的氧化产物,将溶液中的Cu2+除尽后,进行了如下实验。可选用的试剂KSCN 溶液、K3[Fe(CN)6]溶液、氯水。
请完成下表:
操作 | 反应或现象 | 结论 |
(1)取少量除尽 Cu2+后的溶液于试管中,加入__溶液,振荡 | 现象____ | 存在 Fe3+ |
(2)取少量除尽 Cu2+后的溶液于试管中,加入 K3[Fe(CN)6]溶液,振荡 | 离子方程式____ | 存在 Fe2+ |
Ⅱ.Cu(NO3)2 的热稳定性
在如图所示的实验装置A 中,用酒精喷灯对Cu(NO3)2 固体加强热,产生红棕色气体,在装置C中收集到无色气体,经验证为O2。当反应结束以后,试管中残留固体为红色。


(1)装置B 的作用是_______ 。
(2)从实验安全角度考虑,需要在A、B 间加入装置M,请在方框中画出M 装置。_________
(3)下图为Cu(NO3)2 样品高温过程的热重曲线(样品质量分数w%随温度变化的曲线)。Cu(NO3)2 加热到200℃的化学方程式为___________ ,继续高温至1000℃生成_______(填化学式)固体。
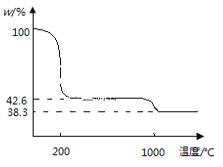 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钛被誉为“21世纪的金属”,可呈现多种化合价.其中以+4价的Ti最为稳定.回答下列问题:
(1)基态Ti原子的价电子轨道表示式为________.
(2)已知电离能:I2(Ti)=1310kJ/mol,I2(K)=3051kJ/mol.I2(Ti)<I2(K),其原因为________.
(3)钛某配合物可用于催化环烯烃聚合,其结如下图所示:
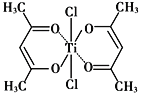
①铁的配位数为________,碳原子的杂化类型________.
②该配合物中存在的化学键有________(填字母标号).
a.离子健 b.配位键 c.金属健 d.共价键 e.氢键
(4)钛与卤素形成的化合物熔沸点如下表所示:
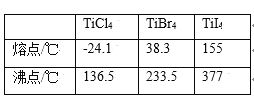
分析TiCl4、TiBr4、TiI4的熔点和沸点呈现一定变化规律的原因是________.
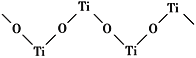
(5)已知TiO2与浓硫酸反应生成硫酸氧钛,硫酸氧钛晶体中阳离子为链状聚合形式的离子,结构如图所示,该阳离子化学式为____.阴离子的空间构型为____.
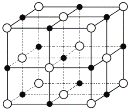
(6)已知TiN晶体的晶胞结构如下图所示,若该晶胞的密度ρg/cm3,阿伏加德罗常数值为NA则晶胞中Ti原子与N原子的最近距离为________pm.(用含ρ、NA的代数式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:[FeCl4(H2O)2]-为黄色,下列实验所得结论不正确的是
① | ② | ③ | ④ |
0.1mol/L Fe2(SO4)3溶液 |
酸化的0.1mol/L Fe2(SO4)3溶液 |
酸化的0.1mol/L Fe2(SO4)3溶液 |
0.1mol/L FeCl3溶液 |
加热前溶液为浅黄色,加热后颜色变深 | 加热前溶液接近无色,加热后溶液颜色无明显变化 | 加入NaCl后,溶液立即变为黄色,加热后溶液颜色变深 | 加热前溶液为黄色,加热后溶液颜色变深 |
注:加热为微热,忽略体积变化。
A. 实验①中,Fe2(SO4)3溶液显浅黄色原因是Fe3+水解产生了少量Fe(OH)3
B. 实验②中,酸化对Fe3+水解的影响程度大于温度的影响
C. 实验③中,存在可逆反应: Fe3+ + 4Cl-+ 2H2O ![]() [FeCl4(H2O)2]-
[FeCl4(H2O)2]-
D. 实验④,可证明升高温度,Fe3+水解平衡正向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)1molO3的质量为________,O2的摩尔质量为________,2molO3和3molO2的质量之比为_____,分子数之比为_____,同温同压下的密度之比为_____.含氧原子数之比为_____.
(2)10.6gNa2CO3溶于水配成500mL 溶液,物质的量浓度为_________,其中Na+的物质的量浓度为________。
(3)标准状况下11.2LHCl气体的物质的量为________,所含氢原子与________g CH4中的氢原子数相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知298.15 K时,可逆反应:Pb2+(aq)+Sn(s)![]() Pb(s)+Sn2+(aq)的平衡常数K=2.2,若溶液中Pb2+和Sn2+的浓度均为0.10 mol·L-1,则此时反应进行的方向是
Pb(s)+Sn2+(aq)的平衡常数K=2.2,若溶液中Pb2+和Sn2+的浓度均为0.10 mol·L-1,则此时反应进行的方向是
A. 向正反应方向进行 B. 向逆反应方向进行
C. 处于平衡状态 D. 无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图。已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的非金属性在同周期元素中最强。下列说法不正确的是

A. 对应简单离子半径X<W
B. 对应气态氢化物的稳定性Y<Z
C. 化合物XZW既含离子键也含共价键
D. Y的氧化物能与Z或X的最高价氧化物对应的水化物反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com